题目内容
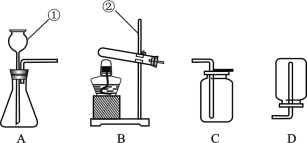
【题目】(6分)下图甲、乙、丙、丁四只手分别代表H2SO4、CuSO4、Fe、Ca(OH)2四种物质中的一种,紧握的两只手表示对应的物质在常温下能发生反应。根据要求回答问题:

(1)_________与其他三种物质不属于同一类物质。
(2)用CuSO4与Ca(OH) 2配制农药波尔多液时,不能用铁桶盛装,其原因用化学方程式表示________。
(3)若图中甲为H2SO4,则丙是 。
【答案】(1)Fe(2)Fe+CuSO4=FeSO4+Cu(3)CuSO4
【解析】
试题分析:(1)铁属于单质,而其他三种属于化合物;(2)用CuSO4与Ca(OH) 2配制农药波尔多液时,不能用铁桶盛装,其原因用化学方程式表示Fe+CuSO4=FeSO4+Cu;(3)图中甲物质为硫酸,丙为硫酸铜,因为硫酸铜在常温下不与稀硫酸发生反应。

【题目】(13分)中和反应是一类重要的反应。根据要求回答问题:
(1)许多物质在溶液中以离子形式存在。下图表示HCl、NaOH溶液及两者混合后溶质在溶液中的存在情况。
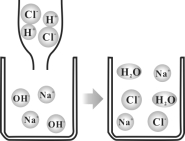
①盐酸具有酸的特性,是因为盐酸溶液中含有 (填微粒符号)。
②对比分析盐酸与氢氧化钠溶液混合前后溶液离子存在情况,可知两者反应时不会减少的离子是 。
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失。请结合上图并从微粒的角度分析,盐酸与氢氧化钠反应时,为何酸、碱各自的特性都消失?答: 。
(2)日常生活中,凡是使酸的酸性消失或碱的碱性消失的反应均被称为“中和”。如使用碳酸氢钠(其溶液显碱性)治疗胃酸(主要成分为盐酸)过多症,就因碳酸氢钠能使胃酸的酸性消失,而称为碳酸氢钠“中和”了过多的胃酸。现有碳酸氢钠溶液、酚酞溶液和盐酸溶液,设计实验证明碳酸氢钠溶液与盐酸反应时,碳酸氢钠溶液的碱性、盐酸的酸性都将各自消失。
操作 | 现象 | 结论 |
实验1:往装有碳酸氢钠溶液的试管中先加入2-3滴酚酞溶液,再逐滴加入盐酸直至恰好完全反应 | 滴入酚酞时的现象: ; 逐滴加入盐酸的现象: ________________。 | 两者反应时,碳酸氢钠溶液碱性消失 |
实验2: | 两者反应时,盐酸溶液酸性消失 |