题目内容
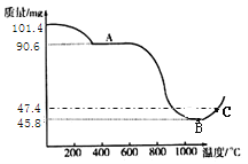
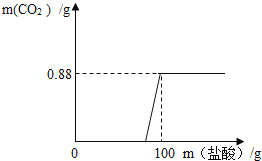
【题目】有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,只放出二氧化碳气体且质量与加入稀盐酸的质量关系如右图所示.试求:
(1)样品中碳酸钠的质量是___g?
(2)样品与足量的稀盐酸反应后生成氯化钠的质量是___g?
(3)样品中氢氧化钠的质量分数是___?
【答案】2.12g 11.7g 64%
【解析】
从坐标系中可以得出生成二氧化碳气体的质量为0.88g,反应一段时间之后才产生气体,说明氢氧化钠是部分变质,从而可以判断所发生的反应为氢氧化钠和盐酸、碳酸钠和盐酸这样的两个反应,解答时可以根据二氧化碳气体的质量,结合碳酸钠和稀盐酸反应的化学方程式,求算出碳酸钠的质量、生成的氯化钠的质量以及消耗盐酸的质量,然后在根据氢氧化钠和盐酸的反应求出氢氧化钠等物质的质量,可以据此解答。
解:(1)设样品中碳酸钠的质量为x,碳酸钠消耗的盐酸的质量为y,同时生成氯化钠的质量为z,
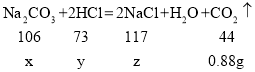
![]()
![]() x=2.12g,
x=2.12g,
![]() y=1.46g,
y=1.46g,
![]() z=2.34g,
z=2.34g,
(2)反应中一共消耗了100g盐酸,所以与氢氧化钠反应的盐酸的质量为:100g×7.3%﹣1.46g=5.84g;设氢氧化钠的质量为m,氢氧化钠与盐酸反应生成氯化钠的质量为n,
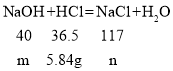
![]() m=6.4g,
m=6.4g,
![]() n=9.36g,
n=9.36g,
结合(1)的解答可以知道反应中一共生成的氯化钠的质量为:2.34g+9.36g=11.7g;
(3)样品中氢氧化钠的质量分数为:![]() ×100%=64%;
×100%=64%;
答:(1)样品中碳酸钠的质量是2.12g;
(2)样品与足量的稀盐酸反应后生成氯化钠的质量是11.7g;
(3)样品中氢氧化钠的质量分数是64%。

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目