题目内容
【题目】某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).查阅资料可知Mg、Mg3N2能发生如下反应:①2Mg+O2![]() 2MgO; ②3Mg+N2
2MgO; ②3Mg+N2![]() Mg3N2; ③2Mg+CO2
Mg3N2; ③2Mg+CO2![]() 2MgO+C;④Mg+H2O
2MgO+C;④Mg+H2O ![]() MgO+H2↑; ⑤Mg3N2+6H2O
MgO+H2↑; ⑤Mg3N2+6H2O ![]() 3Mg(OH)2↓+2NH3↑.
3Mg(OH)2↓+2NH3↑.
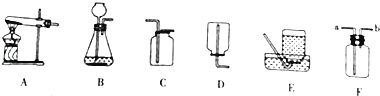
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连).回答下列问题: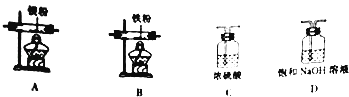
(1)连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是→→B→(填装置序号).D装置中发生反应的化学方程式为 .
(2)通气后,应向点燃(填“A”或“B”)装置的酒精灯,如果同时点燃A、B装置的酒精灯,对实验结果有何影响? .
(3)设计一个实验,验证产物是氮化镁:
实验操作和实验现象 | 实验结论 |
产物是氮化镁 |
(4)思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气正燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释 .
【答案】
(1)D;C;A;CO2+2NaOH═Na2CO3+H2O
(2)B;制得的氮化镁不纯
(3)将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝
(4)O2比N2化学性质活泼
【解析】(1)根据题中信息可知Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2 , 浓硫酸作用是除去水蒸气,浓氢氧化钠是除去空气中二氧化碳,灼热的铁粉为了除去空气中氧气;除去水蒸气选用浓硫酸,除去氧气用能与空气中氧气反应的物质即可,除去二氧化碳用氢氧化钙溶液吸收,但要先除去二氧化碳再干燥然后除去氧气,所以答案是:D→C→B→A;二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.(2)通气后,应向点燃B装置的酒精灯,如果同时点燃A、B装置的酒精灯,A没有排完空气就加热会让空气中的氧气、氮气和水与镁反应生成其他物质,制得的氮化镁不纯;(3)依据氮化镁和水反应生成氨气,方程式为 Mg3N2+6H2O=3Mg(OH)2+2NH3↑,将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁;(4)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2 , 因为O2比N2化学性质活泼.
答案:(1)D→C→B→A;CO2+2NaOH═Na2CO3+H2O.(2)B;制得的氮化镁不纯;(3)
实验操作和实验现象 | 实验结论 |
将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝 | 产物是氮化镁 |
4)O2比N2化学性质活泼.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

 阅读快车系列答案
阅读快车系列答案