题目内容
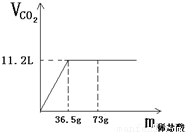
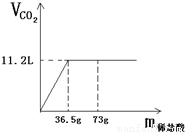
现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如下图所示.试回答:
(1)该石灰石样品最多可以制取CO2______ g;(结果取整数,CO2的密度为1.98g/L)
(2)该石灰石样品中碳酸钙的质量分数是多少?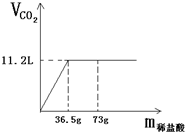
(1)该石灰石样品最多可以制取CO2______ g;(结果取整数,CO2的密度为1.98g/L)
(2)该石灰石样品中碳酸钙的质量分数是多少?

(1)二氧化碳的质量=1.98g/L×11.2L=22g
(2)设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 22g
=
x=50g
该石灰石样品中碳酸钙的质量分数=
×100%=62.5%
答:(1)二氧化碳的质量为22g,(2)石灰石样品中碳酸钙的质量分数为62.5%
故答案为:(1)22(2)62.5%
(2)设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 22g
| 100 |
| x |
| 44 |
| 22g |
x=50g
该石灰石样品中碳酸钙的质量分数=
| 50g |
| 80g |
答:(1)二氧化碳的质量为22g,(2)石灰石样品中碳酸钙的质量分数为62.5%
故答案为:(1)22(2)62.5%

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
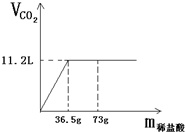 现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如下图所示.试回答:
现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如下图所示.试回答: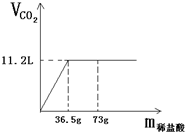 现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如下图所示.试回答:
现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如下图所示.试回答: