题目内容
 实验是进行科学探究的重要途径.在一次实验探究课上,同学们自己动手对氢氧化钠的性质进行了探究,请你参与他们的活动并填写以下空白.
实验是进行科学探究的重要途径.在一次实验探究课上,同学们自己动手对氢氧化钠的性质进行了探究,请你参与他们的活动并填写以下空白.
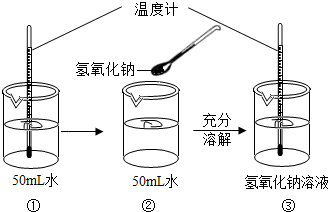
活动一:探究氢氧化钠固体溶于水是否放热?
(1)小林同学按如图所示过程进行溶解实验,看到③中温度计示数明显升高,由此得出的结论是________;
(2)小海同学在另一个实验台上同时也做了这个实验,但观察到温度计示数没有发生明显变化,请你分析其原因可能是:________(只答一点).
活动二:探究氢氧化钠溶液与二氧化碳气体是否发生反应?
(3)小林同学用如图所示的实验仪器与药品进行活动二的探究,实验步骤如下表,请你预测实验现象并解释产生此现象的原因.
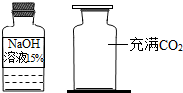
| 实验步骤 | 预测实验现象 | 产生此现象的原因 |
| 向集气瓶中倒入少量的氢氧化钠溶液,立即盖好玻璃片,振荡,将集气瓶倒置,把扶在玻璃片上的手移开,使其悬空. |
(5)在小林实验的基础上,请你自选药品帮助设计一个补充实验,证明氢氧化钠溶液与二氧化碳气体确实发生了反应________________.(写出实验步骤、实验现象).
解:(1)根据图示可以看出,③温度计的示数明显升高,说明有热量放出,所以本题答案为:氢氧化钠固体溶于水放热;
(2)氢氧化钠固体溶于水放出的热量是固定的,温度变化是否明显与所取固体的量和水的量有关,另外药品变质也会影响热量的放出,所用的仪器也会影响测定的效果,所以本题答案为:固体质量取得不足(或水加多了或药品变质或取错药品或温度计坏了等,合理即可);
(3)氢氧化钠与二氧化碳反应,使气体被消耗,集气瓶内压强减小,倒置集气瓶,玻璃片不掉落,所以本题答案为:玻璃片不掉落,瓶内气体减少,压强变小;
(4)小林的实验不足以证明氢氧化钠溶液与二氧化碳气体确实发生了反应,是因为二氧化碳会溶于水,所以本题答案为:二氧化碳溶解于水(或与水反应;
(5)证明氢氧化钠溶液与二氧化碳气体确实发生了反应,就是证明碳酸钠的存在,而碳酸盐具有遇酸化气和与含可溶性钙、钡离子的物质反应生成沉淀的性质,所以本题答案为:用试管取少量集气瓶中的液体,向其中加入适量稀盐酸(或氯化钙溶液或氢氧化钙溶液或氯化钡溶液或氢氧化钡溶液或用塑料瓶和试管等做对比实验,合理即可),有气泡产生(或有白色沉淀产生)(其它答案合理即可)
分析:氢氧化钠固体溶于水要放出大量的热,温度变化是否明显与所用固体的量和水的量有关;氢氧化钠与二氧化碳发生化学反应会生成碳酸钠,要设计实验证明二者确实发生了化学反应,就是证明碳酸钠的存在,因此可以从碳酸盐的检验着手解题.
点评:本题考查了氢氧化钠的性质,在设计实验室,要注意物质的量的多少对实验结果的影响,设计实验证明氢氧化钠与二氧化碳发生了化学反应,其实质就是考查的碳酸盐的检验,同学们要注意从现象中抽取解题的本质.
(2)氢氧化钠固体溶于水放出的热量是固定的,温度变化是否明显与所取固体的量和水的量有关,另外药品变质也会影响热量的放出,所用的仪器也会影响测定的效果,所以本题答案为:固体质量取得不足(或水加多了或药品变质或取错药品或温度计坏了等,合理即可);
(3)氢氧化钠与二氧化碳反应,使气体被消耗,集气瓶内压强减小,倒置集气瓶,玻璃片不掉落,所以本题答案为:玻璃片不掉落,瓶内气体减少,压强变小;
(4)小林的实验不足以证明氢氧化钠溶液与二氧化碳气体确实发生了反应,是因为二氧化碳会溶于水,所以本题答案为:二氧化碳溶解于水(或与水反应;
(5)证明氢氧化钠溶液与二氧化碳气体确实发生了反应,就是证明碳酸钠的存在,而碳酸盐具有遇酸化气和与含可溶性钙、钡离子的物质反应生成沉淀的性质,所以本题答案为:用试管取少量集气瓶中的液体,向其中加入适量稀盐酸(或氯化钙溶液或氢氧化钙溶液或氯化钡溶液或氢氧化钡溶液或用塑料瓶和试管等做对比实验,合理即可),有气泡产生(或有白色沉淀产生)(其它答案合理即可)
分析:氢氧化钠固体溶于水要放出大量的热,温度变化是否明显与所用固体的量和水的量有关;氢氧化钠与二氧化碳发生化学反应会生成碳酸钠,要设计实验证明二者确实发生了化学反应,就是证明碳酸钠的存在,因此可以从碳酸盐的检验着手解题.
点评:本题考查了氢氧化钠的性质,在设计实验室,要注意物质的量的多少对实验结果的影响,设计实验证明氢氧化钠与二氧化碳发生了化学反应,其实质就是考查的碳酸盐的检验,同学们要注意从现象中抽取解题的本质.

练习册系列答案
相关题目