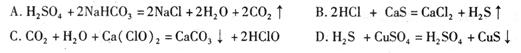题目内容
除去下表物质中含有的杂质,所选试剂不正确的是( )| 选项 | 物质 | 杂质 | 除去杂质所选试剂 |
| A | 铜粉 | 铁 | 硫酸铜溶液 |
| B | 生石灰 | 碳酸钙 | 稀盐酸 |
| C | 氧气 | 二氧化碳 | 氢氧化钠溶液 |
| D | 稀硝酸 | 硫酸 | 硝酸钡溶液 |
A.A
B.B
C.C
D.D
【答案】分析:A、根据金属活动性顺序进行分析;
B、根据生石灰会与水反应进行分析;
C、根据酸性氧化物会与碱反应进行分析;
D、根据硫酸会与硝酸钡反应进行分析.
解答:解:A、混合物中加入硫酸铜,铁会与硫酸铜反应生成硫酸亚铁和铜,过滤后就只剩下铜,故A正确;
B、盐酸会与氧化钙和碳酸钙反应,除去杂质时,也会出去主要物质,故B错误;
C、混合气通过氢氧化钠后,二氧化碳会与氢氧化钠反应而被吸收,最后就只剩氧气,故C正确;
D、硫酸和硝酸钡反应生成硫酸钡沉淀和硝酸,过滤后,就只剩硝酸了,故D正确.
故选B.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.
B、根据生石灰会与水反应进行分析;
C、根据酸性氧化物会与碱反应进行分析;
D、根据硫酸会与硝酸钡反应进行分析.
解答:解:A、混合物中加入硫酸铜,铁会与硫酸铜反应生成硫酸亚铁和铜,过滤后就只剩下铜,故A正确;
B、盐酸会与氧化钙和碳酸钙反应,除去杂质时,也会出去主要物质,故B错误;
C、混合气通过氢氧化钠后,二氧化碳会与氢氧化钠反应而被吸收,最后就只剩氧气,故C正确;
D、硫酸和硝酸钡反应生成硫酸钡沉淀和硝酸,过滤后,就只剩硝酸了,故D正确.
故选B.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.

练习册系列答案
相关题目
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.小平和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题.
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸.下列反应均能发生,其中不符合该规律的是 (填字母
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
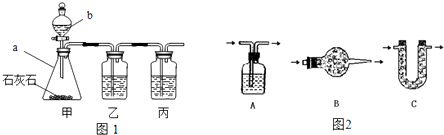
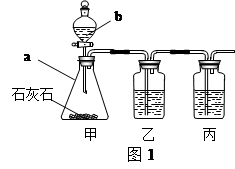
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
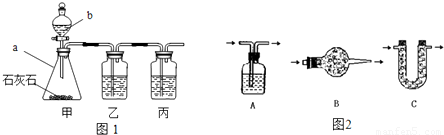
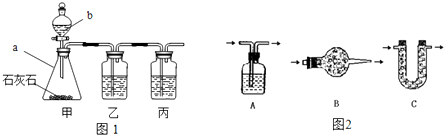
[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是 ,仪器b的名称是 .装置甲中主要反应的化学方程式为 .
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去 .装置丙中主要反应的化学方程式为 .装置乙中盛有的物质是 溶液.现象: .
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品 (选择序号);若选用B装置,则B装置中放入药品 (选择序号).
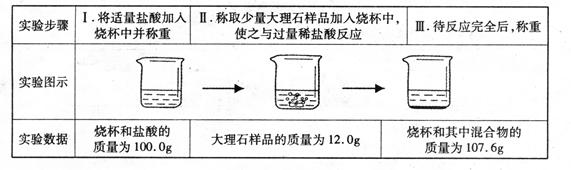
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
小明同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g.大理石样品纯度为83.3%.请你评价他的结论是否正确 ,并简述理由 .
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:

[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是 ,仪器b的名称是 .装置甲中主要反应的化学方程式为 .
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去 .装置丙中主要反应的化学方程式为 .装置乙中盛有的物质是 溶液.现象: .
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品 (选择序号);若选用B装置,则B装置中放入药品 (选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
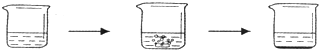
| 实验步骤 | I将适量盐酸加入烧杯中并称量 | II称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.小平和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题.
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸.下列反应均能发生,其中不符合该规律的是 (填字母
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是 ,仪器b的名称是 .装置甲中主要反应的化学方程式为 .
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去 .装置丙中主要反应的化学方程式为 .装置乙中盛有的物质是 溶液.现象: .
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品 (选择序号);若选用B装置,则B装置中放入药品 (选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
小明同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g.大理石样品纯度为83.3%.请你评价他的结论是否正确 ,并简述理由 .
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:

[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是 ,仪器b的名称是 .装置甲中主要反应的化学方程式为 .
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去 .装置丙中主要反应的化学方程式为 .装置乙中盛有的物质是 溶液.现象: .
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品 (选择序号);若选用B装置,则B装置中放入药品 (选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
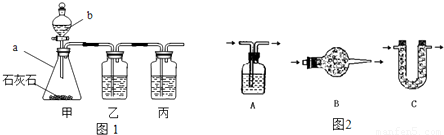
| 实验步骤 | I将适量盐酸加入烧杯中并称量 | II称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样的质量为12.0g | 烧杯和其中混合物的质量为107.6g |