题目内容
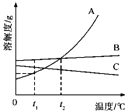
【题目】对知识的归纳和总结是学好科学的重要方法.在学习了酸碱的性质后,小红同学总结了稀盐酸和氢氧化钙的化学性质(如图),


(1)为了验证氢氧化钙与酸碱指示剂反应,小红将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变成____________色
(2)利用氢氧化钙与碳酸钠反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该化学反应的方程式______________________.
(3)利用稀盐酸的化学性质,可以去除铁锈,请写出方程式_______________________
(4)老师告诉同学们:对于酸和盐的反应,可以用厨房中的常见物品进行实验,其中能发生反应的两种物品是 和 (填名称或俗称)。
(5)工业上采用石灰浆雾滴技术除去废气中的二氧化硫,在此对石灰浆进行雾化处理的目的是________________________
【答案】(1)红 (2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH (3)Fe2O3+6HCl=2FeCl3+3H2O (4)醋 食用碱(或纯碱) (5)增大石灰浆与二氧化硫的接触面积,提高吸收率。
【解析】
试题分析:(1)碱性溶液能使无色酚酞变红色;(2)氢氧化钙溶液能够与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠溶液,反应可以表示为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;(3)稀盐酸能够与氧化铁反应生成氯化铁和水,反应的方程式为Fe2O3+6HCl=2FeCl3+3H2O;(4)厨房中的酸为醋酸、盐为碳酸钠或纯碱;(5)工业上采用石灰浆雾滴技术除去废气中的二氧化硫,在此对石灰浆进行雾化处理的目的是增大石灰浆与二氧化硫的接触面积,提高吸收率。

【题目】(7分)有人提出运用高科技可以使水变成汽油,小明认为可以用物质组成的观点揭开这个骗局。以下是小明的实验探究过程。
【提出问题】根据水的组成和汽油的组成判断,水是否可以变成汽油?
【猜想与验证】(1)探究水的组成。实验装置示意图如图:
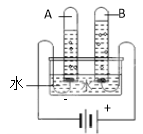
(1)通电一段时间后,经过检验可知,试管A中的气体是 。该反应的符号表达式为 。该实验说明:水是由 组成的(写名称)。
(2)探究汽油的组成。
实验操作如下:
实验步骤 | 实验现象 | 实验目的 |
①点燃使用汽油作燃料的油灯 |
| |
②将光洁干冷的小烧杯罩在油灯火焰的上方 | 现象:小烧杯内壁出现小水珠 | 证明汽油在空气中燃烧后的产物中有水 |
③将内壁蘸有 的小烧杯罩在油灯火焰的上方 | 现象: | 证明汽油在空气中燃烧后的产物中有二氧化碳 |
该实验说明:汽油的组成中肯定含有的元素有 (写元素符号)。
【得出结论】因为汽油和水的组成元素不同,所以水不能变成汽油。