题目内容
【题目】化学兴趣小组的同学不慎将一小片镁片掉落到水中,观察到镁片表面有少量气泡产生。他们对此展开了探究:
(提出问题)镁与水能否反应?若反应,产物是什么?
(查阅资料)①镁与水能反应,生成氢氧化镁和氢气;②氢氧化镁难溶于水,受热易分解,生成两种氧化物。
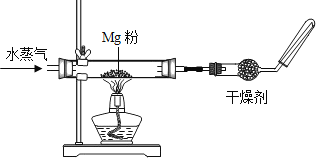
(实验方案)同学们设计了如图装置:
(1)向装置中通入水蒸气目的是______,给玻璃管加热,收集气体,然后______,听到轻微的爆鸣声,证明产物中有氢气。
(2)取少量反应后的固体放入热水中,充分搅拌,向水中滴加2滴无色酚酞溶液,溶液变______色,说明溶液显碱性。
(实验结论)写出镁与水反应生成氢氧化镁与氢气的化学方程式______,属于______反应。
(评价与反思)在此条件下,玻璃管中生成的固体还含有氧化镁,原因是______(用化学方程式解释)。
(3)镁在热水中的反应速率比冷水中的快,可能的原因是______。
还有哪些因素影响镁和水反应的速率?请提出你的猜想,并设计实验验证:
(猜想)______。
(实验方案)______。
【答案】提供反应物 用拇指堵住试管口,移近火焰,松开拇指点火 红 Mg+2H2O=Mg(OH)2+H2↑ 置换 ![]() 温度越高反应速率越快 镁的形状 取等质量的镁粉和镁条放入试管中,再分别加入等体积相同温度的水,观察现象
温度越高反应速率越快 镁的形状 取等质量的镁粉和镁条放入试管中,再分别加入等体积相同温度的水,观察现象
【解析】
[实验方案]
(1)该实验的目的是探究镁与水能否反应,水是反应物,所以向装置中通入水蒸气目的是提供反应物;给玻璃管加热,收集气体,然后用拇指堵住试管口,移近火焰,松开拇指点火,听到轻微的爆鸣声,证明产物中有氢气。
故填:提供反应物;用拇指堵住试管口,移近火焰,松开拇指点火。
(2)酚酞遇碱变红色,取少量反应后的固体放入热水中,充分搅拌,向水中滴加2滴无色酚酞溶液,溶液变红色,说明溶液显碱性。
故填:红。
[实验结论]
镁与水反应生成氢氧化镁与氢气的化学方程式为:Mg+2H2O=Mg(OH)2+H2↑,该反应是单质与化合物反应生成单质和化合物,属于置换反应。
故填:Mg+2H2O=Mg(OH)2+H2↑;置换。
[评价与反思]
加热条件下,生成的氢氧化镁受热分解氧化镁和水,所以玻璃管中生成的固体还含有氧化镁。
故填:![]() 。
。
(3)镁在热水中的反应速率比冷水中的快,可能的原因是温度越高反应速率越快。
故填:温度越高反应速率越快。
[猜想]镁的形状影响反应速率;
[实验方案]取等质量的镁粉和镁条放入试管中,再分别加入等体积相同温度的水,观察现象。
故填:镁的形状;取等质量的镁粉和镁条放入试管中,再分别加入等体积相同温度的水,观察现象。