题目内容
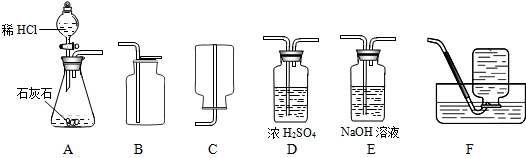
某实验小组为了除去铜丝网上的黑色物质(CuO),进行铜丝网的回收再利用,制定了如下两种方案。请根据方案回答:(提示:黑色铜丝网是铜和氧化铜混合物)
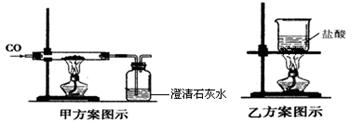
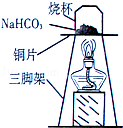
(1)甲方案的玻璃管中发生反应的化学方程式是 ,其中氧化铜失去氧,发生了 (填“氧化”或“还原”)反应。乙方案的烧杯中现象是 ,发生反应的化学方程式是_ 。两种方案相比较,甲方案明显的不足之处是 。
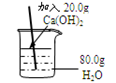
(2)若两种方案中加入的试剂均过量,则甲方案中回收的铜丝网的质量(填“<”、“>”、“=”) 乙方案中回收的铜丝网的质量。
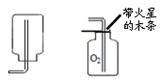
(3)反应结束后,写出能证明乙方案中盐酸过量的实验操作和现象是 。
(4)若在乙方案反应后烧杯中的液体中加入足量的铁粉充分搅拌,最后得到的溶液中溶质为 。

(1)甲方案的玻璃管中发生反应的化学方程式是 ,其中氧化铜失去氧,发生了 (填“氧化”或“还原”)反应。乙方案的烧杯中现象是 ,发生反应的化学方程式是_ 。两种方案相比较,甲方案明显的不足之处是 。
(2)若两种方案中加入的试剂均过量,则甲方案中回收的铜丝网的质量(填“<”、“>”、“=”) 乙方案中回收的铜丝网的质量。
(3)反应结束后,写出能证明乙方案中盐酸过量的实验操作和现象是 。
(4)若在乙方案反应后烧杯中的液体中加入足量的铁粉充分搅拌,最后得到的溶液中溶质为 。
(1)CuO+CO 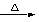 Cu+CO2 ;还原 ;固体溶解,溶液呈蓝色。CuO + 2HCl → CuCl2 + H2O ;没有尾气处理(或污染环境,合理给分)(2) > ;
Cu+CO2 ;还原 ;固体溶解,溶液呈蓝色。CuO + 2HCl → CuCl2 + H2O ;没有尾气处理(或污染环境,合理给分)(2) > ;
(3)取样于试管中,加入Fe(或Zn等活泼金属),产生气泡。
取样于试管中,加入碳酸钠(或碳酸盐),产生气泡。
取样于试管中,加入氧化铜(或氧化铁),固体溶解。
取样于试管中,加入氢氧化铜(或氢氧化铁),固体溶解。(合理即可)
(4)FeCl2(或氯化亚铁)
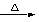 Cu+CO2 ;还原 ;固体溶解,溶液呈蓝色。CuO + 2HCl → CuCl2 + H2O ;没有尾气处理(或污染环境,合理给分)(2) > ;
Cu+CO2 ;还原 ;固体溶解,溶液呈蓝色。CuO + 2HCl → CuCl2 + H2O ;没有尾气处理(或污染环境,合理给分)(2) > ;(3)取样于试管中,加入Fe(或Zn等活泼金属),产生气泡。
取样于试管中,加入碳酸钠(或碳酸盐),产生气泡。
取样于试管中,加入氧化铜(或氧化铁),固体溶解。
取样于试管中,加入氢氧化铜(或氢氧化铁),固体溶解。(合理即可)
(4)FeCl2(或氯化亚铁)
试题分析:(1)甲方案的玻璃管中发生反应的化学方程式是CuO+CO
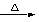 Cu+CO2 其中氧化铜失去氧,发生了还原反应,乙方案的烧杯中现象是固体表面变为紫红色,溶液由无色变为蓝色,发生反应的化学方程式是CuO + 2HCl → CuCl2 + H2O ;两种方案相比较,甲方案明显的不足之处是操作复杂,没有尾气处理装置;(2)若两种方案中加入的试剂均过量,则甲方案中回收的铜丝网的质量大于乙方案中回收的铜丝网的质量,因为甲中的氧化铜转化为铜,而乙中的氧化铜反应为氯化铜进入溶液;(3)反应结束后,能证明乙方案中盐酸过量的实验操作和现象是方案设计就是利用酸的5条化学性质取用不同试剂进行验证,故取样于试管中,加入Fe(或Zn等活泼金属),产生气泡。
Cu+CO2 其中氧化铜失去氧,发生了还原反应,乙方案的烧杯中现象是固体表面变为紫红色,溶液由无色变为蓝色,发生反应的化学方程式是CuO + 2HCl → CuCl2 + H2O ;两种方案相比较,甲方案明显的不足之处是操作复杂,没有尾气处理装置;(2)若两种方案中加入的试剂均过量,则甲方案中回收的铜丝网的质量大于乙方案中回收的铜丝网的质量,因为甲中的氧化铜转化为铜,而乙中的氧化铜反应为氯化铜进入溶液;(3)反应结束后,能证明乙方案中盐酸过量的实验操作和现象是方案设计就是利用酸的5条化学性质取用不同试剂进行验证,故取样于试管中,加入Fe(或Zn等活泼金属),产生气泡。取样于试管中,加入碳酸钠(或碳酸盐),产生气泡。
取样于试管中,加入氧化铜(或氧化铁),固体溶解。
取样于试管中,加入氢氧化铜(或氢氧化铁),固体溶解。均可以,(4)若在乙方案反应后烧杯中的液体中加入足量的铁粉充分搅拌,最后得到的溶液中溶质为氯化亚铁,因为铁能与盐酸反应也能与氯化铜反应生成氯化亚铁。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目