题目内容
【题目】实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:_____。
小王同学对“双氧水分解快慢的影响因素”进行了探究。
(提出问题)影响双氧水分解快慢的因素有哪些?
(猜想与假设)猜想一:可能与二氧化锰的形状有关;猜想二:可能与反应温度有关。
(设计并实验)小王同学用8ml 3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2有剩余):
实验编号 | 温度/℃ | 二氧化锰的形状(均取0.1g) | 收集到氧气的体积/ml(时间均为10s) |
① | 20 | 块状 | a |
② | 20 | 粉末状 | b |
③ | 30 | 块状 | c |
④ | 30 | 粉末状 | d |
(1)欲探究温度对“双氧水分解快慢”是否有影响,应该比较_____和_____(填“a”“b”“c”或“d”)的大小;若粉末状二氧化锰催化效果好,那么_____>_____(填“a”“b”“c”或“d”)。
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证_____。
(3)小王同学还使用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响,他在8mL3%的双氧水中分别加入了0.03g、0.06g、0.08g、0.12g、0.24gMnO2,测得容器内压强的变化曲线如图所示(曲线的斜率代表征催化反应的速半),请你观察图示并写出两条规律性结论:
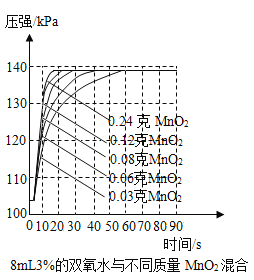
①_____。②_____。
【答案】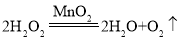 a(或b) c(或d) b(或d) a(或c) 相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积 一定范围内,二氧化锰用量越多,双氧水分解越快 一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响
a(或b) c(或d) b(或d) a(或c) 相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积 一定范围内,二氧化锰用量越多,双氧水分解越快 一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响
【解析】
双氧水在二氧化锰催化条件下制取氧气,写出相关反应的化学方程式: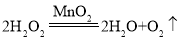 。
。
(1)欲探究温度对”双氧水分解快慢“是否有影响,应该比较a和c,这是因为a和c中,二氧化锰都是块状,温度不同;也可以比较b和d,这是因为b和d中,二氧化锰都是粉末状,温度不同;若粉末状二氧化锰催化效果好,相同温度下,粉末状的反应快,相同时间收集的氧气体积大,故对于①②比较:b>a;对于③④比较:d>c。
(2)相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积。
(3)由图中信息可知:一定范围内,二氧化锰用量越多,双氧水分解越快;一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响。

 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案