题目内容
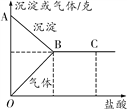
【题目】有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样品溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,现象如图所示(ABC表示沉淀变化,OBC表示气体变化)。
(1)由此推断原白色固体中一定含有什么?
(2)在C点时,所得溶液中的溶质一定有什么?
(3)小红认为还需验证此白色固体中是否还含有另一种物质,请你写出所需的实验操作。
【答案】(1)碳酸钠、硫酸钠、氯化钡;(2)氯化钡、氯化氢;(3)加少量水,感受温度是否升高,如果温度升高,则白色固体中还含有氢氧化钠。
【解析】(1)将固体溶解于水,硫酸钠会与氯化钡反应生成硫酸钡沉淀,硫酸钡不溶于盐酸;碳酸钠会与氯化钡反应生成碳酸钡沉淀,碳酸钡沉淀会溶于盐酸,据图可以看出,加入盐酸,沉淀减少,然后不变,且有气体生成,故一定含有碳酸钡沉淀和硫酸钡沉淀,所以混合物中一定含有碳酸钠、硫酸钠和氯化钡;(2)因为硫酸钠会与氯化钡反应生成硫酸钡沉淀和氯化钠;碳酸钠会与氯化钡反应生成碳酸钡沉淀和氯化钠;碳酸钡沉淀会溶于盐酸生成二氧化碳和氯化钡、水,盐酸时过量的,故在C点时,所得溶液中的溶质一定有氯化钡、氯化氢;(3)为了验证此白色固体中是否还含有氢氧化钠,则:加少量水,感受温度是否升高,如果温度升高,则白色固体中还含有氢氧化钠。

练习册系列答案
相关题目
