题目内容
【题目】工业上制金属钛采用金属热还原法还原四氯化钛。将钛铁矿和炭粉混合加热进行氯化处理,并使生成的TiCl4在高温下用熔融的镁在氩气中反应可得多孔的海绵钛,这种海绵钛经过粉碎、放入真空电弧炉里熔炼,最后制成各种钛材。下图为某化工企业生产流程示意图: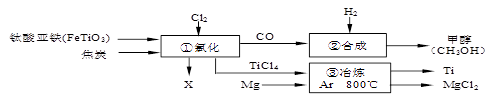
请回答下列问题:
(1)钛酸亚铁(FeTiO3)中钛元素的化合价为。
(2)①中的反应为:2FeTiO3+6C+7Cl2 ![]() 2X+2TiCl4+6CO,则X为(填化学式)。
2X+2TiCl4+6CO,则X为(填化学式)。
(3)③中需要氩气(Ar)作保护气,请写出③中反应的化学方程式 , 并推测钛的一点化学性质。
(4)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为。
【答案】
(1)+4
(2)FeCl3
(3)TiCl4+2Mg ![]() Ti+2MgCl2,钛易与氧气反应
Ti+2MgCl2,钛易与氧气反应
(4)7∶1
【解析】解:(1)化合物中各元素的化合价代数和为0,亚铁显+2价,Ti设为x,O显-2价,那么(+2×1)+(x×1)+ (-2×3)=0,x=+4;(2)由质量守恒定律,反应前后原子的种类和数目不变,以此可得2X含有2Fe,6Cl,那么X含有Fe和3Cl,以此为FeCl3;(3) 为镁与氯化钛反应置换出钛,TiCl4 +2Mg ![]() Ti +2MgCl2;需要用保护气,那么说明钛易与氧气反应;(4) 一氧化碳和氢气反应生成甲醇,方程式为
Ti +2MgCl2;需要用保护气,那么说明钛易与氧气反应;(4) 一氧化碳和氢气反应生成甲醇,方程式为
CO+ | 2H2=CH3OH |
28 | 4 |
以此一氧化碳和氢气的质量比=28:4=7∶1。
所以答案是:(1)+4;(2)FeCl3;(3)TiCl4+2Mg![]() Ti+2MgCl2;钛易与氧气反应;7∶1。
Ti+2MgCl2;钛易与氧气反应;7∶1。
【考点精析】关于本题考查的质量守恒定律及其应用和书写化学方程式、文字表达式、电离方程式,需要了解①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏;注意:a、配平 b、条件 c、箭号才能得出正确答案.

【题目】分类是一种简单有效的科学方法。小强对所学知识进行归纳,其中甲包含了乙、丙、丁。下列关系中没有错误的一组是
甲 | 乙 | 丙 | 丁 | |
A | 常见的空气污染物 | 二氧化碳 | 二氧化硫 | 一氧化碳 |
B | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
C | 常见的干燥剂 | 氢氧化钠 | 生石灰 | 浓硫酸 |
D | 常见的合成材料 | 塑料 | 合金 | 合成纤维 |
A. AB. BC. CD. D