题目内容
【题目】空气是一种宝贵的自然资源,人类无时无刻离不开空气。通过一段时间的化学学习,我们已经了解了空气中氧气的性质与制法,请结合所学知识回答下列问题:
(1)下列有关氧气的叙述正确的是_________
A 氧气的化学性质比较活泼,是可燃物
B 氧气在低温、高压的条件下可以转变为液体或固体
C 给氯酸钾加热,若不加二氧化锰就不产生氧气
D 因为氧气与氮气的密度不同,所以工业上分离液态空气法制取氧气
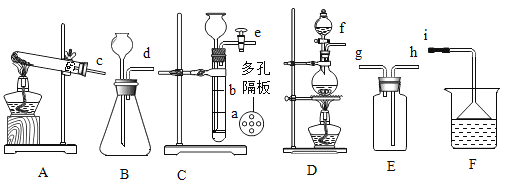
(2)实验室制取氧气,可供选择的实验装置如图所示。
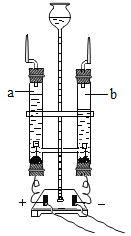
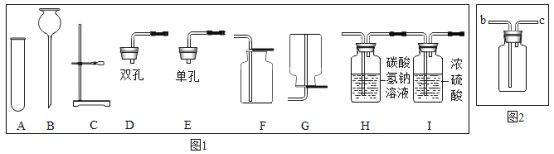
①写出图中标号的仪器名称:a___________。
②写出一个用B装置制取氧气的化学方程式___________;若将B、C装置组装在一起制氧气,实验结束,停止加热前要先进行的操作是______________。
③若用过氧化氢溶液和二氧化锰制取氧气,应选用的发生装置是__________(填字母)。在加试剂之前的操作是______________。
④已知一氧化氮气体的密度比空气略大,难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置___________(填字母)。
(3)加热分解6.3克高锰酸钾,可以得到氧气的质量是多少_________?(计算结果保留一位小数)
【答案】B 分液漏斗 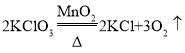 先把导管移出水面,再熄灭酒精灯 A 检验装置气密性 C 0.6g
先把导管移出水面,再熄灭酒精灯 A 检验装置气密性 C 0.6g
【解析】
(1)A、氧气的化学性质比较活泼,但是不具有可燃性,该选项叙述不正确;
B、氧气在低温、高压的条件下可以转变为液体或固体,该选项叙述正确;
C、给氯酸钾加热,若不加二氧化锰也能够产生氧气,只不过产生氧气的速率慢一些,该选项叙述不正确;
D、因为氧气与氮气的沸点不同,所以工业上可以通过分离液态空气法制取氧气,该选项叙述不正确.
故填:B。
(2)①a是分液漏斗,通过分液漏斗可以向锥形瓶中注入液体药品。
②因为试管口没有塞一团棉花,应该用加热氯酸钾和二氧化锰的混合物制取氧气,氯酸钾在二氧化锰的催化作用下受热分解的化学方程式为: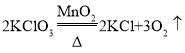 ;
;
停止制氧气时应进行的操作是先把导管移出水面,再熄灭酒精灯,这样可以防止水倒流入试管,把试管炸裂;
③若用过氧化氢溶液和二氧化锰制取氧气,不需加热,故选发生装置A,在加试剂之前要检查装置的气密性,防止装置漏气;
④已知一氧化氮气体的密度比空气略大,难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用排水法,选:C。
(3)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,根据高锰酸钾的质量可以计算生成氧气的质量。
设生成氧气的质量为x,
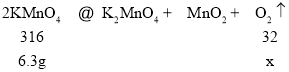
![]()
解得:x≈0.6g,
生成氧气的质量是0.6g。

【题目】下表列出了1~18号元素的原子序数和元素符号
原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
元素符号 | H | He | Li | Be | B | C | N | O | F |
原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
(1)1~18号元素中属于稀有气体元素的有______![]() 填元素符号
填元素符号![]() 。
。
(2) 1~18号元素中最外层有3个电子的原子有______![]() 填元素符号
填元素符号![]() 。
。
(3)某元素的原子结构示意图为 ,它在化学反应中一般易______
,它在化学反应中一般易______![]() 填“得到”或“失去”
填“得到”或“失去”![]() 电子,它与地壳中含量最多的金属元素形成化合物的化学式为______。
电子,它与地壳中含量最多的金属元素形成化合物的化学式为______。