题目内容
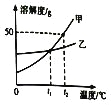
【题目】右图是向50g溶质质量分数为8.0%的氢氧化钠溶液中加入溶质质量分数为10%的稀硫酸至过量的pH变化曲线图,根据图回答以下问题:
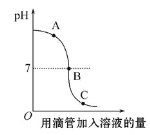
(1)A点时,溶液中的含有的阴离子是_____;
(2)求恰好反应时消耗稀硫酸的质量。_____
【答案】OH-和SO4 2- 4.9g
【解析】
根据图可以看出是向50g溶质质量分数为8.0%的氢氧化钠溶液中加入溶质质量分数为10%的稀硫酸至过量,A点时显示碱性,为氢氧化钠过量,而B点时pH=7恰好完全反应,根据氢氧化钠的质量和对应的化学方程式求算稀硫酸中溶质的质量。
解:(1)在A点时,pH大于7,为氢氧化钠有剩余,所以此时的溶质为剩余的氢氧化钠和生成的硫酸钠,对应的阴离子的化学式为OH-和SO4 2-;
(1)由于50g溶质质量分数为8.0%的氢氧化钠溶液中含有的氢氧化钠的质量为50g×8.0%=4g,设稀硫酸中溶质的质量为x,
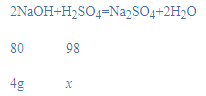
![]()
x=4.9g;
答:(1)A点时,溶液中的含有的阴离子是 OH-和SO4 2-;
(2)恰好反应时消耗稀硫酸的质量是4.9g。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】甲烷是家用天然气的主要成分,它的开发和利用给人们的生活带来了很大的便利,但是天然气使用不当时,也会引发极大的灾害。几位同学想探究甲烷燃烧时会生成哪些物质,请帮助他们完成以下实验探究。
(提出问题)甲烷在氧气中燃烧后生成哪些物质?
(查阅资料)含碳元素的物质在氧气中完全燃烧生成CO2不完全燃烧生成CO;无水CuSO4遇水会由白色变为蓝色。
(猜想与假设)
产物 猜想 | 甲 | 乙 | 丙 | 丁 |
CO2、H2O | CO、H2O | NH3、CO2、H2O | CO2、CO、H2O |
(1)你认为______同学的猜想是错误的,理由是______。
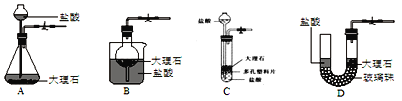
(实验探究)为了验证上述猜想与假设将甲烷在一定量的氧气中燃烧的产物依次通过下列装置:
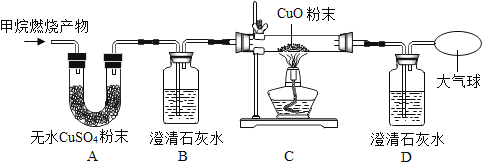
(2)A、B装置的顺序______颠倒(填“能”或“不能”),原因是:______。
(3)实验中用纯净氧气而不用空气的原因是______。
(4)实验中观察到A中现象是______,B,D中澄清石灰水变浑浊,C中现象是______,由此推断丁同学猜想成立。
(5)请写出C中发生的化学反应方程式:______,B中发生的化学反应方程式为______。
(反思与交流)
(6)大气球的作用是______,还可以换成______。
(7)为避免天然气燃烧生成有毒气体,请你给使用天然气的家庭提出建议______。