题目内容
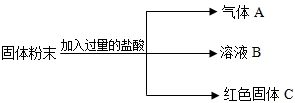
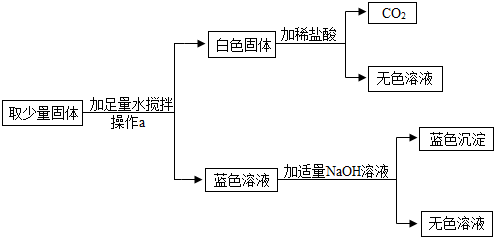
有一包固体粉末,可能含有碳酸钙、硫酸铜、硝酸钾、硫酸钠、氯化钡中的一种或几种.为确定其组成,进行如下实验:(1)取该固体粉末少量加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;
(2)过滤,在白色沉淀中加入足量稀硝酸,白色沉淀不溶解.根据以上实验可推断原固体粉末中不能确定的物质是
分析:根据碳酸钙难溶于水会溶于酸,硫酸铜在溶液中显蓝色,硫酸钡沉淀不溶于水也不溶于酸进行分析.
解答:解:解:取该固体粉末少量加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液,可以确定没有硫酸铜,白色沉淀中加入足量的稀硝酸,白色沉淀不溶解,说明白色沉淀不是碳酸钙,是硫酸钡,说明混合物中没有碳酸钙,有氯化钡和硫酸钠,硝酸钾对上面的实验现象不会产生影响,所以无法确定硝酸钾的存在,
设生成4.66克的沉淀需要氯化钡x,硫酸钠y,
BaCl2+Na2SO4=2NaCl+BaSO4↓
208 142 233
x y 4.66g
=
═
x=4.16g y=2.84g
故氯化钡和硫酸钠的质量之和为:7克,反应物的质量和等于预设质量,所以不存在硝酸钾.
故答案为:氯化钡;硫酸钠
设生成4.66克的沉淀需要氯化钡x,硫酸钠y,
BaCl2+Na2SO4=2NaCl+BaSO4↓
208 142 233
x y 4.66g
| 208 |
| x |
| 142 |
| y |
| 233 |
| 4.66g |
x=4.16g y=2.84g
故氯化钡和硫酸钠的质量之和为:7克,反应物的质量和等于预设质量,所以不存在硝酸钾.
故答案为:氯化钡;硫酸钠
点评:在解此类题时,首先要弄清楚混合物中各种物质的性质,然后根据题中的现象进行逐一的对照分析.
在根据化学方程式计算时,书写方程式,列出比例式是关键.
在根据化学方程式计算时,书写方程式,列出比例式是关键.

练习册系列答案
相关题目