题目内容
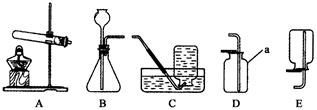
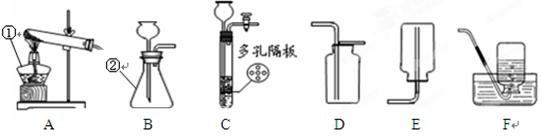
(8分)甲、乙、丙三位同学在活动课上利用下图所示装置制取常见的气体,请根据题意回答下列问题。
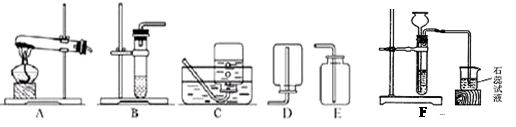
(1)甲同学用加热氯酸钾和二氧化锰的固体混合物制取O2,发生装置应选用上图中的________装置(填编号),该反应的化学方程式为______________ ____________;若用C装置收集,当O2收集满并取出集气瓶后,停止该实验的正确操作方法是
________ ________。
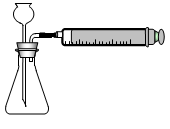
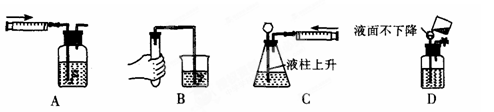
(2)乙同学利用B装置制取CO2,下图是乙同学在化学实验中主要操作过程的示意图。
 根据上述实验操作过程,。请找出乙同学的操作错误的是(填序号)__________、 。
根据上述实验操作过程,。请找出乙同学的操作错误的是(填序号)__________、 。
(3)丙同学用浓盐酸与大理石在F装置中制取CO2并检验其有关性质,写出制取CO2的化学方程式_____________ ___________________,实验中观察到烧杯内紫色石蕊试液变红,请你分析使紫色石蕊试液变红的原因可能有:
①___________________
___________________ 。
②___________________
___________________ 。

(1)甲同学用加热氯酸钾和二氧化锰的固体混合物制取O2,发生装置应选用上图中的________装置(填编号),该反应的化学方程式为______________ ____________;若用C装置收集,当O2收集满并取出集气瓶后,停止该实验的正确操作方法是
________ ________。
(2)乙同学利用B装置制取CO2,下图是乙同学在化学实验中主要操作过程的示意图。
 根据上述实验操作过程,。请找出乙同学的操作错误的是(填序号)__________、 。
根据上述实验操作过程,。请找出乙同学的操作错误的是(填序号)__________、 。(3)丙同学用浓盐酸与大理石在F装置中制取CO2并检验其有关性质,写出制取CO2的化学方程式_____________ ___________________,实验中观察到烧杯内紫色石蕊试液变红,请你分析使紫色石蕊试液变红的原因可能有:
①___________________
___________________ 。
②___________________
___________________ 。
(1)A (1分) 2KClO3 2KCl + 3O2↑ (1分)
2KCl + 3O2↑ (1分)
先将导管移出水面,再熄灭酒精灯(1分)
(2)Ⅱ(1分) Ⅳ(1分)
(3)CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O (1分)
①产生的CO2与H2O反应生成H2CO3,使石蕊试液变红(1分)
②挥发出的氯化氢溶于水,使石蕊试液变红(1分)
 2KCl + 3O2↑ (1分)
2KCl + 3O2↑ (1分)先将导管移出水面,再熄灭酒精灯(1分)
(2)Ⅱ(1分) Ⅳ(1分)
(3)CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O (1分)
①产生的CO2与H2O反应生成H2CO3,使石蕊试液变红(1分)
②挥发出的氯化氢溶于水,使石蕊试液变红(1分)
(1)氯酸钾和二氧化锰制取氧气需加热,故应选固体加热制气装置A,其化学方程式为2KClO3 2KCl + 3O2↑,装置C为排水集气法,应先将导管移出水面,再熄灭酒精灯,避免水倒流使试管炸裂。
2KCl + 3O2↑,装置C为排水集气法,应先将导管移出水面,再熄灭酒精灯,避免水倒流使试管炸裂。
(2)操作Ⅱ错误,瓶塞不应正放在桌面上,会沾有杂物污染试剂,应倒放在桌面上;
操作Ⅳ错误,燃着的火柴应放在瓶口不应伸入集气瓶。
(3)盐酸与大理石反应生成氯化钙、水和二氧化碳,其方程式为CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O;紫色石蕊遇酸变红色,其原因可能有①产生的CO2与H2O反应生成H2CO3,使石蕊试液变红②该反应使用的是浓盐酸具有挥发性,挥发出的氯化氢溶于水形成盐酸,使石蕊试液变红。
 2KCl + 3O2↑,装置C为排水集气法,应先将导管移出水面,再熄灭酒精灯,避免水倒流使试管炸裂。
2KCl + 3O2↑,装置C为排水集气法,应先将导管移出水面,再熄灭酒精灯,避免水倒流使试管炸裂。(2)操作Ⅱ错误,瓶塞不应正放在桌面上,会沾有杂物污染试剂,应倒放在桌面上;
操作Ⅳ错误,燃着的火柴应放在瓶口不应伸入集气瓶。
(3)盐酸与大理石反应生成氯化钙、水和二氧化碳,其方程式为CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O;紫色石蕊遇酸变红色,其原因可能有①产生的CO2与H2O反应生成H2CO3,使石蕊试液变红②该反应使用的是浓盐酸具有挥发性,挥发出的氯化氢溶于水形成盐酸,使石蕊试液变红。

练习册系列答案
相关题目
 (1)A图中制取CO2的化学方程式为 ,浓硫酸的作用是 。
(1)A图中制取CO2的化学方程式为 ,浓硫酸的作用是 。