题目内容
【题目】继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起。为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得钯金和铁的氯化物。经分析所得钯金的质量为10.6g,未反应的铁粉质量为4.4g,下列说法正确的是( )
A. 生成铁的氯化物质量为![]() B. 生成铁的氯化物质量为
B. 生成铁的氯化物质量为![]()
C. 该反应说明钯金比铁活泼D. 生成铁的氯化物为![]()
【答案】A
【解析】
A、PdCl2和铁反应生成氯化亚铁和钯;100gPdCl2溶液中含有质量为:100g×17.7%=17.7g,参加反应的PdCl2的质量是17.7g,参加反应的铁的质量是10.0g-4.4g=5.6g,生成钯金的质量为10.6g,根据质量守恒定律可知,生成铁的氯化物质量为:17.7g+5.6g-10.6g=12.7g,故A正确;
B、由上述计算可知,生成铁的氯化物质量为12.7g,不是16.25g,故B错误;
C、由题意可知,铁能将钯从其盐溶液中置换出来,说明铁比钯活泼,故C错误。
D、生成铁的氯化物为FeCl2,不是FeCl3,故D错误。故选A。

 优生乐园系列答案
优生乐园系列答案【题目】下列实验操作、现象和结论对应正确的是( )
实验操作 | 现象 | 结论 | |
A | 向久置于空气中的NaOH溶液滴加稀H2SO4 | 有气泡产生 | NaOH和H2SO4发生了化学反应 |
B | 向某溶液中滴加BaCl2溶液 | 有白色沉淀 | 原溶液含有SO42﹣ |
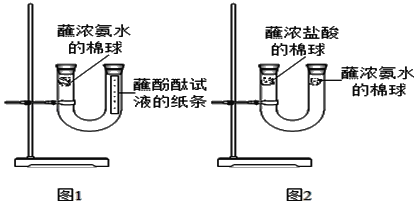
C | 向集满CO2的软塑料瓶中加入约 | 塑料瓶变瘪, 溶液变红 | CO2能与石蕊反应 |
D | 将质量相同的Mg、Zn分别投入到足量的稀HCl中 | 镁条表面产生气体更多、更快 | 金属活动性:Mg>Zn |
A. AB. BC. CD. D
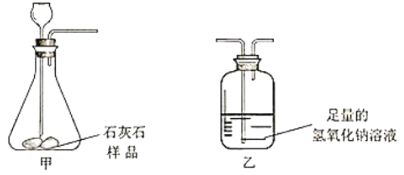
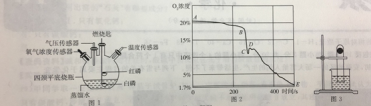
【题目】某化学兴趣小组做了如图所示实验,当向乙烧杯中依次加入MnO2和H2O2溶液时,发现有大量气泡产生,并产生大量白雾,蜡烛燃烧更旺,但过一会儿逐渐熄灭。而甲烧杯中蜡烛一直持续燃烧。
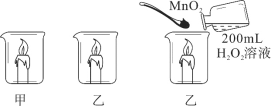
(知识回忆)写出过氧化氢分解产生氧气的化学方程式:_____。
(问题1)导致乙烧杯中蜡烛熄灭的原因是什么?
(作出猜想)猜想一:燃烧产生的CO2使蜡烛熄灭;
猜想二:白雾是水雾导致蜡烛熄灭;
小组同学经过讨论,排除了猜想一,其理由是_____。
(实验1)向一只装有燃者蜡烛的烧杯中加入100℃水,另一只依次加入MnO2和H2O2溶液,若观察到_____的现象,则猜想二正确。
(查阅资料)水雾产生与H2O2溶液的溶质质量分数大小有关,并且H2O2溶液的溶质质量分数越大,产生的水雾越多。
(问题2)为什么H2O2溶液的溶质质量分数越大水雾越多呢?
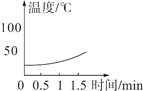
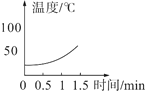
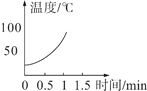
(实验2)分别向三只烧杯依次加入MnO2和溶质质量分数的不同H2O2溶液测定温度变化。
H2O溶液 | 5% | 10% | 30% |
温度变化曲线 |
|
|
|
(解释与结论)
(1)该对比实验过程中不需要控制的条件是_____。
A H2O2溶液的初始温度相同 B 反应开始的时间相同 C 二氧化锰的质量相同
(2)根据实验2,可得出的一个结论是_____。