题目内容
【题目】下图中是氧元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
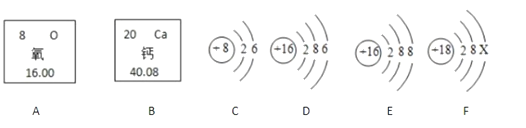
请你回答:
(1)氧元素的原子序数为_____。
(2)E粒子属于_____(填“原子”“阴离子”或“阳离子”),该粒子的符号为_____。
(3)F元素在元素周期表中的位置处于第_____周期
(4)写出由B、C、D三种元素组成的化合物的化学式____。
【答案】8 阴离子 S2- 三 CaSO4
【解析】
由结构示意图可知,C为氧原子,D为硫原子,E为硫离子,F为氩原子。
(1)元素周期表左上角数字表示原子序数。由图可得,氧元素的原子序数为8。
(2)原子核内质子带正电,核外电子带负电。已知E粒子核外电子数比核内质子数多2,所以E粒子带2个负电荷。
(3)在原子中,核电荷数=核外电子数,若所给粒子为原子,则18-2+8+X,X=8,则F元素的原子的核外电子层数为3,在元素周期表中的位置处于第三周期。
(4)B为钙元素;C原子的核电荷数为8,为氧元素,D 原子的核电荷数为16,为硫元素。则三者可组成硫酸钙, 化学式为CaSO4。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】KCl与KNO3在不同温度的溶解度数据如表.则下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
A.KNO3比KCl的溶解度大
B.两物质的溶解度相等的温度在20~30℃之间
C.在20℃时,10g水中加入5g KCl可得到33.3%的KCl溶液
D.在50℃时,两物质各5g分别加入10g水中,充分溶解,均有固体剩余
【题目】酒精是一种无色、透明、有特殊气味的液体,易挥发,能与水以任意比互溶,常用作酒精灯和内燃机的燃料,是一种绿色能源,当点燃酒精灯时,酒精在灯芯上气化后燃烧生成水和二氧化碳。
(1)根据以上叙述,可归纳出酒精的物理性质是____;化学性质是____;酒精的用途是___。
(2) 实验中,不小心将酒精灯碰倒在桌上燃烧起来,合理简单的灭火措施是_______。
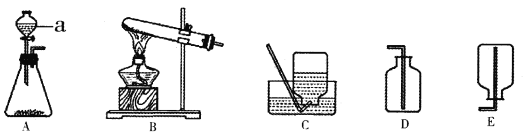
(3)下列仪器不能用酒精灯加热的是(______)
A燃烧匙 B试管 C量筒 D蒸发皿
(4)某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。

① 写出铁丝在氧气中燃烧的化学符号表达式: ___________________________________。
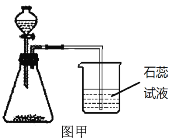
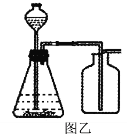
② 探究一:蜡烛燃烧产生火焰的原因是什么? 点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由____________(填“固态”或“气态”)物质燃烧形成的。
③ 探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其____________(填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰________。由此推测:钠在燃烧时,________(填“有”或“没有”)火焰产生。
④ 根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点______硫燃烧时的温度(填“>”或“<”或“=”)
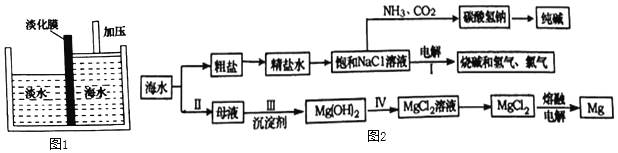
【题目】气在生产、生活中有广泛用途,研究其制取、性质和用途十分重要.
(1)工业上用氮气和氢气在高温高压和催化剂存在时合成氨;实验室用氯化铵和熟石灰在加热条件下制取氨气,同时生成氯化钙和水.请分别写出有关反应的化学方程式___________.实验室制取氨气的发生装置与制取哪种气体的相似,请写出实验室制取该气体的化学方程式:__________
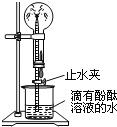
(2)如图是氨气性质的趣味实验:圆底烧瓶中充满氨气,当挤压胶头滴管并打开止水夹时,烧杯中的水迅速进入烧瓶,形成美丽的“喷泉”,进入烧瓶的水变成红色.由该实验可得出哪些结论___________
(3)氨气常作制冷剂及化肥,同时,它还可作清洁能源.已知表信息:
性质 | 颜色、气味 | 沸点(℃) | 25℃水中溶解度(g/L-1) |
NH3 | 无色、刺激性 | -33 | 456 |
H2 | 无色、无味 | -253 | 0.0015 |
一定条件下氨气在纯氧中完全燃烧生成水和氮气,写出该反应的化学方程式______________________.
液氨有望和液氢一样成为新一代绿色能源.与H2相比,用NH3作燃料的优点之一是便于储存和运输;优点之二是泄漏时易发现且便于处理.请对氨气的优点加以解释说明_________________