题目内容
【题目】从分子、原子角度对下面一些现象和变化的解释,合理的是( )
A. 花香四溢 分子很小,质量也很小
B. 热胀冷缩 温度变化,分子或原子大小发生变化
C. 滴水成冰 温度降低,分子间隔变小,停止运动
D. 食品变质 分子发生变化,分子性质发生变化
【答案】D
【解析】
A、花香四溢说明分子之间有间隙,与分子的质量和体积无关,故错误;
B、热胀冷缩是分子之间的间隙变大,分子和原子的大小不变,错误;
C、滴水成冰是由于温度降低,分子间隔变小,分子继续做无规则的运动,错误;
D、食品变质是食品与氧气发生缓慢氧化的过程,分子的性质发生了变化,正确。故选D。

【题目】碳酸镁水合物是制备镁产品的中间体. 【制取MgCO33H2O】工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO33H2O的方法如图1: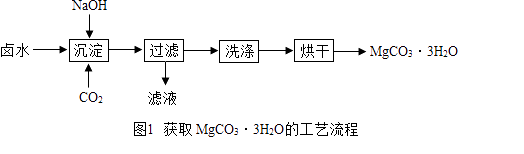
(1)沉淀过程的化学方程式为: MgCl2+CO2+2NaOH+2H2O═MgCO33H2O↓+2 .
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为(填字母). 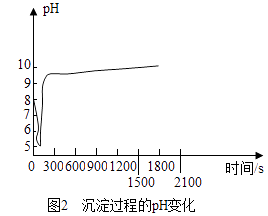
a.向卤水中滴加NaOH溶液,同时通入CO2
b.向NaOH溶液中滴加卤水,同时通入CO2
c.向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
d.向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如表26﹣1所示. 
表26﹣1 不同反应温度下的水合碳酸镁
温度(℃) | 产物 |
46.95 | MgCO33H2O |
47.95 | MgCO33H2O |
48.95 | MgCO33H2O |
49.95 | Mg5(OH)2(CO3)44H2O |
则沉淀过程选择的温度为 , 理由是 .
(4)【测定MgCO33H2O的纯度】 利用如图所示装置(图中夹持仪器略去)进行实验,以确定MgCO33H2O的纯度.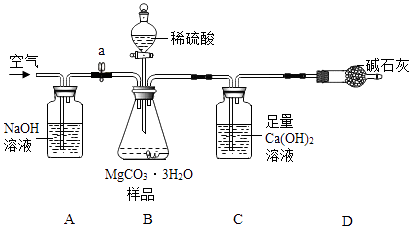
依据实验过程回答下列问题:
实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有 .
(5)C中反应生成CaCO3的化学方程式为;D中碱石灰的作用为 .
(6)下列各项措施中,不能提高测定准确度的是(填标号). a.在加入硫酸之前,应排净装置内的CO2气体
b.为了缩短实验时间,快速滴加硫酸
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在C装置左侧导管末端增添多孔球泡
(7)实验中准确称取15.0g样品三份,进行三次测定,测得中生成CaCO3沉淀的平均质量为10.0g.请计算样品中MgCO33H2O的纯度(写出计算过程).
(8)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有 .
(9)若获取MgCO33H2O的样品中含有少量Mg5(OH)2(CO3)44H2O,则产品中镁元素的质量分数(填“偏大”“不变”或“偏小”,下同),样品中MgCO33H2O的纯度 .