题目内容
(6分)为测定实验室里过氧化氢溶液中溶质的质量分数,同学们取10g过氧化氢溶液入2g二氧化锰,完全反应后,称得剩余物的总质量为11.84g。计算:
(1)生成氧气的质量 g;
(2)过氧化氢溶液中溶质的质量分数。
(1)生成氧气的质量 g;
(2)过氧化氢溶液中溶质的质量分数。
(1)0.16 (1分)
(2)解:设过氧化氢的质量为x
2H2O2 2H2O+O2↑ (1分)
2H2O+O2↑ (1分)
68 32
x 0.16g (1分)
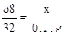 (1分)
(1分)
x=0.34g (1分)
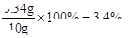 (1分)
(1分)
答:过氧化氢溶液的溶质质量分数为3.4%。
(2)解:设过氧化氢的质量为x
2H2O2
 2H2O+O2↑ (1分)
2H2O+O2↑ (1分)68 32
x 0.16g (1分)
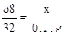 (1分)
(1分)x=0.34g (1分)
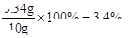 (1分)
(1分)答:过氧化氢溶液的溶质质量分数为3.4%。
(1)根据质量守恒定律,反应前后减少的质量为氧气的质量.
(2)利用分解过氧化氢制氧气的化学方程式,根据氧气的质量求出过氧化氢的质量,根据
过氧化氢的质量/过氧化氢溶液的质量×100%求出过氧化氢溶液中溶质的质量分数.
解:(1)氧气的质量:10g+2g-11.84g=0.16g
故答案为:0.16
(2)设:过氧化氢溶液中过氧化氢的质量为x
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
x 0.16g
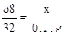
x="0.34g"
过氧化氢溶液中溶质的质量分数为
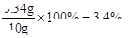
答:过氧化氢溶液的溶质质量分数为3.4%.
点评:本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.
(2)利用分解过氧化氢制氧气的化学方程式,根据氧气的质量求出过氧化氢的质量,根据
过氧化氢的质量/过氧化氢溶液的质量×100%求出过氧化氢溶液中溶质的质量分数.
解:(1)氧气的质量:10g+2g-11.84g=0.16g
故答案为:0.16
(2)设:过氧化氢溶液中过氧化氢的质量为x
2H2O2
 2H2O+O2↑
2H2O+O2↑ 68 32
x 0.16g
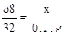
x="0.34g"
过氧化氢溶液中溶质的质量分数为
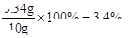
答:过氧化氢溶液的溶质质量分数为3.4%.
点评:本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
相关题目