题目内容
【题目】用下图常用实验装置制取常见的气体,并进行相应性质实验。
实验一:实验室中可用KClO3在MnO2催化下受热分解制取氧气,完全反应后对混合物进行分离回收并进行相关性质实验,实验操作如图所示(MnO2难溶于水)。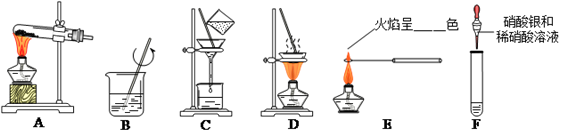
(1)写出图A中发生反应的化学方程式。图B操作的名称是 , 图C操作中的一处明显错误 , 图D操作中,当看到时停止加热。
(2)取C中滤液分别进行如图E、F所示实验,E处透过蓝色钴玻璃观察火焰呈色,F中滴加硝酸银和稀硝酸产生的实验现象是。
(3)实验二: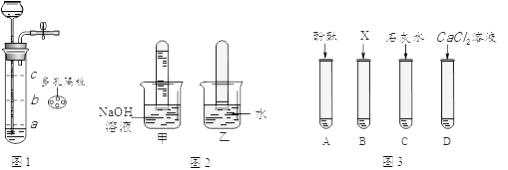
①若用图1装置制取二氧化碳气体,为了便于控制反应随时发生和停止,多孔隔板合适的位置是处(选填“a”、“b”或“c”),不适宜用作多孔隔板的材料是。
A.铁 B.塑料 C.铜片 D.石墨
②用图1装置制取并收集两试管CO2气体,分别倒扣入图2盛有等体积NaOH溶液和水的烧杯中,该组对比实验产生的现象说明。
③为了进一步探究CO2与NaOH溶液是否发生反应,取图2甲烧杯实验后的溶液于图3(A~D)四支试管中,分别滴入四种不同类别的试剂,B中加入的是。四种方案中不合理的是 , 理由是。
【答案】
(1)2KClO3 ![]() 2KCl+3O2↑,溶解,漏斗末端没有紧靠烧杯内壁,有大量固体析出
2KCl+3O2↑,溶解,漏斗末端没有紧靠烧杯内壁,有大量固体析出
(2)紫,白色沉淀
(3)a,A,CO2能与NaOH发生的反应,足量稀HCl/稀HNO3/稀H2SO4,A,NaOH、Na2CO3溶液均显碱性
【解析】本题主要考查实验室制取气体的方法及性质。由题知A中是用氯酸钾反应制氧气,所以化学方程式为:2KClO3 ![]() 2KCl+3O2↑,B图为溶解,C图为过滤,要点 “一贴二低三靠”所以错误之处:漏斗末端没有紧靠烧杯内壁,D图为蒸发,当出现大量固体时就要停止。2、C处中溶质为氯化钾,所以E处放在火焰中为钾的颜色反应为紫色。滴加到F处,氯化钾能与硝酸银反应生成氯化银沉淀,所以填:白色沉淀。
2KCl+3O2↑,B图为溶解,C图为过滤,要点 “一贴二低三靠”所以错误之处:漏斗末端没有紧靠烧杯内壁,D图为蒸发,当出现大量固体时就要停止。2、C处中溶质为氯化钾,所以E处放在火焰中为钾的颜色反应为紫色。滴加到F处,氯化钾能与硝酸银反应生成氯化银沉淀,所以填:白色沉淀。
图1装置为了便于控制反应随时发生和停止,隔板的位置不能离液面太高,所以选:a,制二氧化碳用的是盐酸,所以材料不能与盐酸反应,选:A
将装有二氧化碳的试管倒扣入盛有等体积NaOH溶液和水的 ,在氢氧化钠中液面上升的高,说明能与氢氧化钠反应。 ③二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠属于盐,盐能与金属、酸、碱、盐反应,石灰水属于碱,氯化钙属于盐,所以X是酸。酚酞滴入变为红色,说明有碱性物质,但里在面的氢氧化钠与碳酸钠都是碱性的,所以A不合理。
【考点精析】通过灵活运用过滤操作的注意事项和蒸发操作的注意事项,掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损;蒸发注意点:1、在加热过程中,用玻璃棒不断搅拌2、当液体接近蒸干(或出现较多量固体)时停止加热,利用余热将剩余水分蒸发掉,以避免固体因受热而迸溅出来.3、热的蒸发皿要用坩埚钳夹取,热的蒸发皿如需立即放在实验台上,要垫上石棉网即可以解答此题.

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,为能充分利用钾资源,用饱和的Ca(OH) 2溶液浸杂卤石制备硫酸钾,工艺流程如下: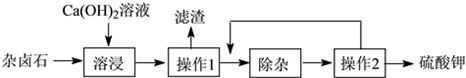
已知:
物质 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作1的名称为 , 所需的玻璃仪器有玻璃棒、烧杯、 , 玻璃棒的作用是。
(2)滤渣的主要成分有和。
(3)“除杂”环节中,先加入 溶液(填字母,下同),经搅拌等操作后,过滤,再加入溶液调滤液pH至中性。
a. K2CO3 b. Na2CO3 c. 稀硫酸 d. 稀盐酸
(4)操作2的步骤是蒸发浓缩、、过滤、洗涤。
(5)洗涤硫酸钾最好选用。
a. 30℃的水 b. 饱和的硫酸钠溶液 c.饱和的硫酸钾溶液