题目内容
 (2006?烟台)用氯气消毒饮用水时,会生成少量对人体有害的有机物.因此,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.ClO2是一种黄绿色、有刺激性气味的气体,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于氯气,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的气味.
(2006?烟台)用氯气消毒饮用水时,会生成少量对人体有害的有机物.因此,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.ClO2是一种黄绿色、有刺激性气味的气体,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于氯气,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的气味.(1)根据以上信息,请你总结出ClO2的性质:
物理性质
黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水
黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水
;化学性质
易与碱反应,见光易分解,有漂白性
易与碱反应,见光易分解,有漂白性
.(2)制取ClO2的方法有多种,目前欧洲一些国家用氯酸钠(NaClO3)与浓盐酸反应制取ClO2(Kestiog法),反应的化学方程式为:2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl.我国最近研究成功用氯气和亚氯酸钠(NaClO2)反应制取ClO2,同时生成一种生活中常见的盐,该反应的化学方程式为
Cl2+2NaClO2=2ClO2+2NaC1
Cl2+2NaClO2=2ClO2+2NaC1
,此法与Kestiog法相比,其优点是无有害气体产生,产品易分离
无有害气体产生,产品易分离
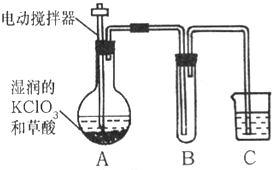
.(3)工业上也可以在60℃时,用稍加潮湿的KClO3与草酸(HOOCCOOH)反应制取ClO2. 某实验小组用右图所示装置制取并收集
ClO2,在装置中A为ClO2的发生装置,B为ClO2收集装置,C为尾气吸收装置.请回答:
①为了保证实验成功,装置A、装置B分别应控制什么条件?
60.0℃、低于11.O℃
60.0℃、低于11.O℃
;你能采取什么方法达到这些条件?A装置置于60℃水浴中,B装置置于冰水中
A装置置于60℃水浴中,B装置置于冰水中
.②C中盛放的液体是
NaOH溶液
NaOH溶液
.分析:(1)根据物质不需要发生化学变化表现出来的性质来分析物理性质,在化学变化中表现的性质为化学性质;
(2)根据氯气和亚氯酸钠(NaClO2)反应制取ClO2,同时生成一种生活中常见的盐,利用元素守恒推测盐,并书写化学反应方程式,然后利用比较得出此方法的优点;
(3)根据反应发生的条件及物质的性质来分析,利用ClO2易与碱反应来分析C中的液体.
(2)根据氯气和亚氯酸钠(NaClO2)反应制取ClO2,同时生成一种生活中常见的盐,利用元素守恒推测盐,并书写化学反应方程式,然后利用比较得出此方法的优点;
(3)根据反应发生的条件及物质的性质来分析,利用ClO2易与碱反应来分析C中的液体.
解答:解:(1)由ClO2是一种黄绿色、有刺激性气味的气体,冷却至11.0℃以下时变成红色液体,易溶于水,这些性质是不需要发生化学变化就克表现出来的性质,
则物理性质有黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水,
由见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于氯气,是在化学变化中表现出来的性质,则化学性质为易与碱反应,见光易分解,有漂白性等,
故答案为:黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水;易与碱反应,见光易分解,有漂白性;
(2)有氯气和NaClO2反应制取ClO2,同时生成一种生活中常见的盐,则由反应前的元素可知盐为氯化钠,则反应为Cl2+2NaClO2=2ClO2+2NaC1,与反应
2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl相比,该反应无有害气体氯气产生,且生成气体和固体产品易分离,
故答案为:Cl2+2NaClO2=2ClO2+2NaC1;无有害气体产生,产品易分离;
(3)①因在60℃时,用稍加潮湿的KClO3与草酸能反应,则A应控制温度在60.0℃,可利用水浴加热的方法里控制,
又ClO2在冷却至11.0℃以下时变成红色液体,为了分离使之变为液体,则B应低于温度11.O℃,可利用冰水来降低温度,
故答案为:60.0℃;低于11.O℃; A装置置于60℃水浴中,B装置置于冰水中;
②由图及ClO2易与碱反应,利用C装置中的液体来吸收气体,则可选择NaOH溶液来吸收ClO2,故答案为:NaOH溶液.
则物理性质有黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水,
由见光易分解.ClO2易与碱反应,其杀菌、漂白能力均优于氯气,是在化学变化中表现出来的性质,则化学性质为易与碱反应,见光易分解,有漂白性等,
故答案为:黄绿色气体,有刺激性气味,沸点11.0℃,液态时呈红色,易溶于水;易与碱反应,见光易分解,有漂白性;
(2)有氯气和NaClO2反应制取ClO2,同时生成一种生活中常见的盐,则由反应前的元素可知盐为氯化钠,则反应为Cl2+2NaClO2=2ClO2+2NaC1,与反应
2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl相比,该反应无有害气体氯气产生,且生成气体和固体产品易分离,
故答案为:Cl2+2NaClO2=2ClO2+2NaC1;无有害气体产生,产品易分离;
(3)①因在60℃时,用稍加潮湿的KClO3与草酸能反应,则A应控制温度在60.0℃,可利用水浴加热的方法里控制,
又ClO2在冷却至11.0℃以下时变成红色液体,为了分离使之变为液体,则B应低于温度11.O℃,可利用冰水来降低温度,
故答案为:60.0℃;低于11.O℃; A装置置于60℃水浴中,B装置置于冰水中;
②由图及ClO2易与碱反应,利用C装置中的液体来吸收气体,则可选择NaOH溶液来吸收ClO2,故答案为:NaOH溶液.
点评:本题较难,学生应注意利用习题中的信息来分析解决问题,并学会利用元素守恒及反应物来推断反应,利用比较的方法分析反应的利弊,注重信息与所学知识的结合是解答的关键.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
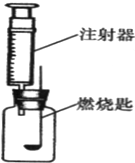 (2006?烟台)请利用水、红磷、量筒和右图所示装置(100mL的注射器、约250mL的广口瓶)测定空气中氧气的体积分数.
(2006?烟台)请利用水、红磷、量筒和右图所示装置(100mL的注射器、约250mL的广口瓶)测定空气中氧气的体积分数.