题目内容
【题目】(1)对比、分析、归纳是学习化学的重要方法。
①已知H2、CO、C是初中化学常见的还原剂,请分析下列反应: H2 + CuO![]() Cu + H2O 3CO + Fe2O3
Cu + H2O 3CO + Fe2O3![]() 2Fe + 3CO2 C + O2
2Fe + 3CO2 C + O2 ![]() CO2 得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后________(选填“升高”或“降低”或“不变”)。
CO2 得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后________(选填“升高”或“降低”或“不变”)。
②依据上述结论,则在反应SO2 + 2H2S = 3S + 2H2O中作为还原剂的物质是________;(填化学式)
(2)按要求写出下列化学方程式:
①电解水____________________________ ②酒精燃烧_________________________ ③碳还原氧化铁______________________ ④检验二氧化碳的反应_____________
【答案】 升高 H2S 2H2O![]() 2H2↑+O2↑ C2H5OH+3O2
2H2↑+O2↑ C2H5OH+3O2![]() 2CO2+3H2O 3C+2Fe2O3
2CO2+3H2O 3C+2Fe2O3![]() 4Fe+3CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O
4Fe+3CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O
【解析】(1)对比、分析、归纳是学习化学的重要方法。①H2、CO、C是初中化学常见的还原剂,在化学反应中失去电子,化合价升高,作还原剂时,所含元素中,一定有元素的化合价在反应后升高。②在反应SO2+2H2S=3S+2H2O中作为还原剂的物质是.H2S,反应前硫元素化合价是-2价,反应后是0价,化合价升高被氧化,属于还原剂。(2)按要求写出下列化学方程式:①电解水是2H2O![]() 2H2↑+O2↑,②酒精燃烧是C2H5OH+3O2
2H2↑+O2↑,②酒精燃烧是C2H5OH+3O2![]() 2CO2+3H2O,③碳还原氧化铁是3 C+2Fe2O3
2CO2+3H2O,③碳还原氧化铁是3 C+2Fe2O3![]() 4Fe+3CO2↑,④检验二氧化碳的反应是.Ca(OH)2+CO2=CaCO3↓+H2O。
4Fe+3CO2↑,④检验二氧化碳的反应是.Ca(OH)2+CO2=CaCO3↓+H2O。
点睛∶化学方程式的书写应遵循的原则是①以客观事实为依据,②遵循质量守恒定律。

【题目】对下列事实的微观解释错误的是
选项 | 事实 | 解释 |
A | 墙内开花墙外香 | 微粒在不断运动 |
B | 工业上用空气制取氧气的过程属于物理变化 | 分子的种类没有发生变化 |
C | H2O、H2O2性质存在明显差异 | 分子的构成不同 |
D | 水蒸发为水蒸气,所占体积变大 | 分子体积变大 |
A.AB.BC.CD.D
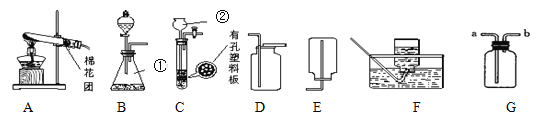
【题目】下图是实验室制取气体的一些装置,据图回答问题(以下所选装置均填装置序号

(1)写出指定仪器的名称①______________;②____________
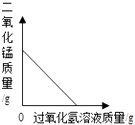
(2)如果用过氧化氢溶液同二氧化锰混合制氧气,要得到较干燥的气体,应选用的气体收集装置是_______________。该反应的化学方程式为______________________
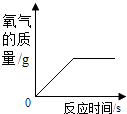
(3)用一定质量的高锰酸钾制取氧气并测量生成气体的体积,反应的化学方程式____________________,整套实验装置接口的正确连接顺序为b→______→______→h。若G装置中水不满,对测量氧气的体积________( 填“有”或“没有”)影响。
(4)解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
小柯:实验测定法 | 小妍:计算法 |
小柯在老师的指导下,将15.8克 高锰酸钾充分加热,得到氧气1300 ml | 解:高锰酸钾中氧元素的质量分数
氧气的质量为:15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g。 |
请回答:
①在本实验条件下,氧气的密度为1.4×l0-3g/mL,则由小柯的测量结果可算出 15.8 g高锰酸钾分解后所产生的氧气质量为 _________________g(结果保留一位小数)。
②大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质量的一项理由是________________(填序号)。
A.高锰酸钾中含氧元素 B.锰酸钾和二氧化锰中含氧元素 C.氧气中含氧元素
③请计算15.8 g高锰酸钾完全分解所产生的氧气质量为_________。(写出解题过程)