题目内容
【题目】盛产石灰石,主要成分是CaCO3。某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取一定量的石灰石样品研碎和100 g溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25 g。)
反应时间/s | 20 | 40 | 60 | 80 | 100 |
烧杯和药品质量/g | 137.8 | 135.6 | m | 134.5 | 134.5 |
请计算:
(1)表中的“m”为________。
(2)该石灰石样品中碳酸钙的质量分数。(计算结果精确至0.1 % )
【答案】(1)134.5;(2)83.3%
【解析】(1)通过分析表中的数据可以看出,反应时间20 s~40 s固体减少了2.2 g,所以40 s~60 s也可能减少2.2 g,反应40 s~80 s,固体质量减少是135.6 g-134.5 g=1.1 g,即60 s前碳酸钙已反应完,则m的值是134.5
(2)解:通过分析表中的数据可知,反应前烧杯的总质量为137.8 g+2.2 g=140 g,所以石灰石样品质量为140 g-100 g-25 g=15 g, 碳酸钙完全反应生成的二氧化碳为140 g-134.5 g=5.5 g。
设石灰石样品中含有碳酸钙的质量为x。
CaCO3+2HCl ===CaCl2+H2O+CO2↑
100 44
x 5.5 g
![]() x=12.5 g
x=12.5 g
碳酸钙的质量分数为:![]() ×100%≈83.3%。
×100%≈83.3%。
答:石灰石样品中碳酸钙的质量分数为83.3%。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
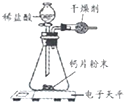
①取研碎后的钙片4克,导入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数.
反应前总质量(克) | 275.58 |
反应后总质量(克) | 274.92 |
反应前后总质量差(克) | 0.66 |
容器内气体质量差(克) | m |
(1)该实验中,对装置中的固态干燥剂的性质有何要求?
(2)反应前容器内是空气(密度为ρ1),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差为m为 .(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑).钙片中的其它成分不与盐酸反应.