题目内容
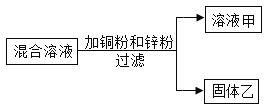
【题目】某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
①固体乙中一定含有Ag,可能含有Cu和Zn
②溶液甲中一定含有Al(NO3)3和Zn(NO3)2
③若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3和Cu(NO3)2
④若溶液甲是无色,则溶液甲一定含有Al(NO3)3、可能有Zn(NO3)2一定没有Cu(NO3)2
⑤向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2
上述四种说法正确的个数为( )
A.1个B.2个C.3个D.4个
【答案】C
【解析】
在金属活动性顺序中:Al>Zn>Cu>Ag,根据排在前面的金属可以把位于它后面的金属从其盐溶液中置换出来,可简记为“前置后,盐可溶”。
根据金属活动性Al>Zn>Cu>Ag,所以锌粉优先与![]() 发生反应,铜粉后与
发生反应,铜粉后与![]() 发生反应,但是铜粉和锌粉都不能和
发生反应,但是铜粉和锌粉都不能和![]() 发生反应,
发生反应,![]() 一定在溶液中;
一定在溶液中;
①锌粉优先与![]() 发生反应生成硝酸锌和银,固体乙中一定含有Ag,可能有Cu和Zn,说法正确;
发生反应生成硝酸锌和银,固体乙中一定含有Ag,可能有Cu和Zn,说法正确;
②锌粉优先与![]() 发生反应生成硝酸锌和银,铜粉和锌粉都不能和
发生反应生成硝酸锌和银,铜粉和锌粉都不能和![]() 发生反应,所以溶液中一定有
发生反应,所以溶液中一定有![]() 和
和![]() ,说法正确;
,说法正确;
③若溶液甲是蓝色,说明铜已经与![]() 发生反应,而锌已经全部反应,溶液甲一定含有
发生反应,而锌已经全部反应,溶液甲一定含有![]() 、
、![]() 和
和![]() ;故说法错误;
;故说法错误;
④若溶液甲是无色,则锌和硝酸银是一定要反应的,溶液中应该一定有硝酸铝、硝酸锌,说法错误;
⑤向固体乙上滴加盐酸有气泡产生,说明固体中有锌,锌过量,铜未参加反应,溶液中![]() 被反应完全,溶液甲中一定没有
被反应完全,溶液甲中一定没有![]() 和
和![]() ,说法正确。
,说法正确。
故①②⑤正确。
故选C.

【题目】某厂废水中含有质量分数为4.9%的H2SO4,需中和后才能排放.某兴趣小组同学经过讨论,提出了两种中和方案,所用试剂的价格如下:
中和试剂 | 氢氧化钠 | 氢氧化钙 |
价格/(元吨﹣1) | 800 | 450 |
(1)请从经济与产物角度说明选择氢氧化钙的理由:
①_____;②_____.
(2)有同学建议用氨水进行中和,可以回收一种化肥,其化学式为_____.该废水还会引起的环境问题是_____(选填编号).
A 重金属污染 B 有毒物质污染 C 富营养化污染 D 悬浮物污染
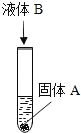
【题目】如图所示,试管中盛有固体物质 A,向试管中加入一种液体物质 B 后,观察 到有气泡产生.请你依据上述实验现象,对 A和 B 的组合至少做出三种猜想(要求三种组合中 的固体 A 分别属于不同类别的物质):
A | B | |
猜想 1 | ____ | ____ |
猜想 2 | ____ | ____ |
猜想 3 | ____ | ____ |