��Ŀ����
����Ŀ����Ҫ��ش����и���
��1��NaBH4��Ϊ��ԭ�������л���ѧ���м�Ϊ�㷺����;��NaBH4�����ܽ���ˮ����ˮ���ò���H2����Ӧ��BԪ����BO2����ʽ��������Һ�У��˷�Ӧ�Ļ�ѧ����ʽΪ��_____��
��2����֪A��B��C��D����ԭ������С��18��Ԫ�أ����ǵ�ԭ��������������B�ĺ˵������A��D�˵����֮�͵�2/3����A�ֱܷ���B��C��D�γɵ���������ȵķ���X��Y��Z����ش��������⣺
��BԪ�ص�������____��C��Ԫ�ط�����______
��Y��C����������������ˮ����պ���ȫ��Ӧʱ����������Ļ�ѧʽΪ_______��
��3����Ԫ�غ�̼Ԫ��һ��Ҳ�����γ�һϵ���⻯�����NH3��N2H4��N3H5��N4H6д����ϵ���⻯���ͨʽ__________________��
���𰸡�NaBH4+2H2O=NaBO2+4H2�� ̼ N NH4NO3 NnHn+2��n��1��
��������
��1���������֪���÷�Ӧ�ķ�Ӧ��ΪNaBH4��ˮ��������Ϊ������NaBO2����˷�Ӧ�Ļ�ѧ����ʽΪ��NaBH4+2H2O=NaBO2+4H2�������NaBH4+2H2O=NaBO2+4H2��
��2��A��B��C��D���ֶ�����Ԫ�ص�ԭ��������������B�ĺ˵������A��D�˵����֮�͵�![]() �������ԭ��������֪��B���ڵڶ����ڣ��Ҵ���ż���壬A�ֱܷ���B��C��D�γɵ���������ȵķ���X��Y��Z������Ϊ�⻯�XΪHԪ�أ�����֪BΪ̼Ԫ�ء�CΪ��Ԫ�أ�DΪ��Ԫ�أ�X��Y��Z�ֱ�ΪCH4��NH3��H2O��
�������ԭ��������֪��B���ڵڶ����ڣ��Ҵ���ż���壬A�ֱܷ���B��C��D�γɵ���������ȵķ���X��Y��Z������Ϊ�⻯�XΪHԪ�أ�����֪BΪ̼Ԫ�ء�CΪ��Ԫ�أ�DΪ��Ԫ�أ�X��Y��Z�ֱ�ΪCH4��NH3��H2O��
�������Ϸ�����֪BΪ̼Ԫ�أ�CΪ��Ԫ�ء����̼����
��Y��C����������������ˮ����ֱ�ΪNH3��HNO3�����պ���ȫ��Ӧʱ����������Ļ�ѧʽΪNH4NO3�����NH4NO3
��3�����ݵ�ԭ�Ӻ���ԭ�Ӹ���֮��Ĺ�ϵ����ԭ�Ӹ����ȵ�ԭ�Ӹ�����2������ͨʽ��ʾΪ��NnHn+2��n��1�������NnHn+2��n��1��

����Ŀ�������̣�Mn�����仯������;�㷺�����̺Ͻ��̸֣������������������ݵ�������ݶ����ϡ����졢�����ȡ������̵Ļ��������ɫ���ܽ��Լ������ش��������⡣
���� | KMnO4 | MnO2 | MnSO4 | Mn(OH)2 | MnO(OH)2 |
��ɫ | ����ɫ | ��ɫ | ��ɫ | ��ɫ | ��ɫ |
�ܽ��� | ���� | ���� | ���� | ���� | ���� |
��1�����ʵ�����������ʯ��Fe2O3�������̿�MnO2������̿��ϼ����¯��ͨ���ȿ����������ɵõ����̺Ͻ��û�ѧ����ʽ��ʾ���ɽ����̵Ĺ��̣�
��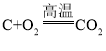 ����______����______��
����______����______��
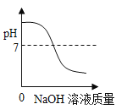
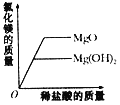
��2����֪����![]() ����
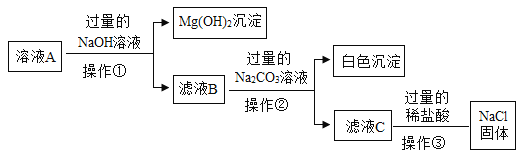
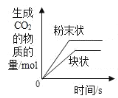
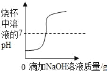
����![]() ������ʢ��MnSO4��Һ���Թ��м�������NaOH��Һ�����ã�Ԥ��ɹ۲쵽��������___��
������ʢ��MnSO4��Һ���Թ��м�������NaOH��Һ�����ã�Ԥ��ɹ۲쵽��������___��
����Ŀ��ij�о�С����MnO2����������ֽ�������������˲�ͬ�������ӶԹ�������ֽ�Ӱ���ʵ�����ϡ�100��ʱ���ڲ�ͬ�������Ӵ����£�����������24h�ķֽ��ʼ��±���
ʵ���� | ���� | ��������mgL-1�� | �ֽ���% |
�� | �� | - | 2 |
�� | Al3+ | 1.0 | 2 |
�� | Fe3+ | 1.0 | 15 |
�� | Cu2+ | 0.1 | 86 |
�� | Cr3+ | 0.1 | 96 |
��ش�
��1��MnO2����������ֽ�Ļ�ѧ����ʽΪ______��
��2��ʵ��ٵ�Ŀ����_____________��
��3��ʵ�������У�����Ũ�ȽϸߵĹ�������ʱ��ʹ�����ޣ��ۣ�����ʹ�ò���ֹޣ��ۣ�����ԭ����_____��