题目内容
【题目】能源与环境已成为人们日益关注的问题。
(1)目前人们利用最多的能源是煤、石油和_________等化石燃料。
(2)汽车使用乙醇汽油可减少对环境的污染,请写出乙醇充分燃烧的方程式:___________
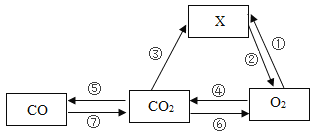
(3)按要求各写出一个有二氧化碳生成的化学方程式:
①置换反应:___________________;②分解反应:__________________ 。
(4)某气体由CH4、C3H4、C3H6中的一种或几种组成,取该气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22∶9,下列对该气体组成判断正确的是____
A 该气体可能是CH4和C3H4 B 该气体中一定没有C3H4
C 该气体可能是CH4和C3H6 D 该气体不可能是C3H6
【答案】天然气 C2H5OH+3O2![]() 2CO2+3H2O C+2CuO
2CO2+3H2O C+2CuO![]() 2Cu+CO2↑ CaCO3
2Cu+CO2↑ CaCO3![]() CaO+CO2↑ A
CaO+CO2↑ A
【解析】
(1)目前人们利用最多的能源是煤、石油和天然气等化石燃料。故填:天然气;
(2)乙醇燃烧生成二氧化碳和水,化学化学方程式为:C2H5OH+3O2![]() 2CO2+3H2O;故填:C2H5OH+3O2
2CO2+3H2O;故填:C2H5OH+3O2![]() 2CO2+3H2O;
2CO2+3H2O;
(3)①碳与氧化铜在高温下反应生成铜和二氧化碳,属于置换反应,反应的化学方程式为:C+2CuO![]() 2Cu+CO2↑;故填:C+2CuO
2Cu+CO2↑;故填:C+2CuO![]() 2Cu+CO2↑;
2Cu+CO2↑;
②碳酸钙高温下分解生成氧化钙和二氧化碳,属于分解反应,反应的化学方程式为:CaCO3![]() CaO+CO2↑;故填:CaCO3
CaO+CO2↑;故填:CaCO3![]() CaO+CO2↑;
CaO+CO2↑;
(4)假设生成二氧化碳质量为22g,则生成水的质量为9g;
22g二氧化碳中C元素质量为22g×![]() =6g,9g水中H元素的质量为9g×
=6g,9g水中H元素的质量为9g×![]() =1g;
=1g;
则可燃物中C、H元素质量比为6g:1g=6:1。
其中C、H原子个数比=![]() :
:![]() =1:2;
=1:2;
CH4中C、H原子个数比=1:4<1:2;
C3H4中C、H原子个数比=3:4>1:2,
C3H6中C、H原子个数比=1:2=1:2;
故选:A。