题目内容
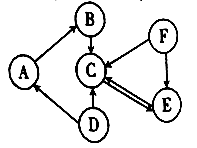
【题目】如图是氧元素、铝元素在周期表中的位置及有关微粒的结构示意图:
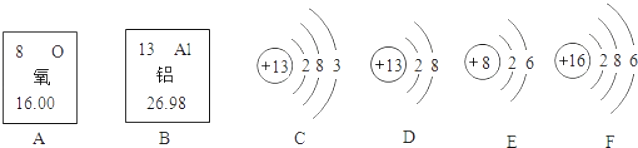
回答下列问题:
(1)氧元素的相对原子质量是_____;图中属于氧原子的结构示意图的是_____;
(2)铝元素的原子序数为_____;属于铝离子的结构示意图是_____;
(3)在CDEF四个结构示意图所代表的微粒化学性质有相似性的一组是_____和_____;
(4)A、B两种元素组成的化合物的化学式为_____.
【答案】16.00 E 13 D E F Al2O3
【解析】
(1)根据元素周期表中的一格中获取的信息,氧元素的相对原子质量是16.00;
根据元素周期表中的一格中获取的信息,氧元素的原子序数为8;由原子序数=核电荷数=质子数,则氧原子的核内质子数为8,E属于氧原子的结构示意图.
(2)根据元素周期表中的一格中获取的信息,铝元素的原子序数为13;由原子序数=核电荷数=质子数,则铝原子的核内质子数为13,C图中质子数=核外电子数=13,为铝原子;质子数=13,核外电子数=10,质子数>核外电子数,为铝离子.
(3)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似;由题目中的信息可知,故E和F的最外层电子数均为6,化学性质有相似性.(4)铝元素和氧元素形成的化合物为氧化铝,其化学式为:Al2O3.
故答案为:(1)16.00;E;(2)13;D;(3)E;F;(4)Al2O3.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】探究影响过氧化氢分解速率的影响因素。
(査阅资料)常温下,H2O2较稳定不易分解;CuSO4溶液、FeCl3溶液和红砖粉末等都能作为H2O2分解制取O2的催化剂。
(分析交流)写出实验室用H2O2溶液和MnO2制取O2的化学方程式:_____。
(实验设计)取相同体积的过氧化氢溶液分别进行下列实验。
实验编号 | 温度/℃ | 催化剂 | 过氧化氢浓度/% |
① | 20 | 无 | 2 |
② | 20 | 无 | 5 |
③ | 20 | 5滴FeCl3溶液 | 5 |
④ | 20 | 5滴CuSO4溶液 | 5 |
(1)实验①②探究的是_____。要探究CuSO4溶液能否做H2O2分解的催化剂,应选择的实验编号是_____。
(2)要定性比较两种催化剂的催化效果,可通过观察_____来实现。要定量比较两者的催化效果,可测量生成等体积气体所需的_____。
(3)同学们实验时还观察到,在H2O2溶液内滴入FeCl3溶液,溶液逐渐由黄色变为浅绿色,最终变回浅黄色。查阅资料得知:FeCl3溶液一般呈黄色,FeCl2溶液一般呈浅绿色。由此你对催化剂有何新的认识?_____。