��Ŀ����
�����Ǵ�����Ⱦ��Σ��֮һ����������SO2���ĺ����ǿ�����������һ����Ҫָ�ꡣij��ȤС��ͬѧ�ռ�ij�ص���ˮ����ʵ�顣
�������Ϣ����ÿ��1 h��ͨ��pH�Ʋⶨ��ˮ��Ʒ��pH����õĽ�����±���
��SO2��ʹƷ����Һ��ɫ��
��pH<5.6����ˮΪ���ꣻ
�ܺ�ˮ�������ԣ�
��BaSO3������ˮ���������ᷴӦ��BaSO4������ˮ��Ҳ���������ᡣ
���������ۡ���������ˮ��pH��Χ�ǣ�7> pH> 5.6��ƫ���ԣ�������Ϊ �� ��
�������ܸ�ʴ������Ʒ���ӻ�����Ӧ�����Ͽ���Ҫ��Ӧ���� �� ��
���ռ���������Ʒ����һ��ʱ���pH��С��ԭ����SO2��ˮ��Ӧ���ɵ�H2SO3������ΪH2SO4����д���÷�Ӧ�Ļ�ѧ����ʽ �� ��
��������롿ͬѧ�ǶԸ��ռ�����������Ʒ�е����ʽ��в��룺
���������������ֻ����H2SO3��
���������������ֻ����H2SO4��
��������������� �� ��
��ʵ��̽����
��1������ռ���������Ʒ�еμӹ���Ba(OH)2��Һ���а�ɫ�������ɣ����ˡ�
������Һ�еμ� �� ��Һ����Һ�� �� ɫ��֤����������Ʒ�еμӵ�Ba(OH)2��Һ�ѹ�����
��������м����������ᣬ���������ܽ��ҷų��д̼�����ζ���塣�÷�Ӧ�Ļ�ѧ����ʽΪ �� �����������й����������ʵIJ��� �� ��ȷ��
��2��ijͬѧȡ������ƷV L������17.1%��Ba(OH)2��Һ�����ٲ�������ʱ��ǡ������10.00 g Ba(OH)2��Һ����V L������Ʒ���ܽ�SO2������Ϊ �� ��
��ʵ�鷴˼����ijЩ�����л��ɷ�������������ڣ��������ڿ����к���ijԪ��+4���������ԭ������������Ļ�ѧʽΪ �� ��
����չ���졿���ú�ˮ�����Ǽ���SO2�ŷŵ���Ч�������乤����������ͼ��ʾ��

��Ȼ��ˮ�����˽϶�ĺ�����������H2SO3���ɣ�H2SO3�뺣ˮ�е����ӷ�Ӧ�����ͷų�CO2��ͨ��������������ˮ������������ǿ��
�����һ�ּ��龻������������Ƿ�SO2�ļ�ʵ�鷽���� �� ��
��������ĺ�ˮ��Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ��ò�������ҪĿ���� �� ��
�������Ϣ����ÿ��1 h��ͨ��pH�Ʋⶨ��ˮ��Ʒ��pH����õĽ�����±���
| �ⶨʱ��/h | 0 | 1 | 2 | 3 | 4 |
| ��ˮ��Ʒ��pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
��pH<5.6����ˮΪ���ꣻ
�ܺ�ˮ�������ԣ�
��BaSO3������ˮ���������ᷴӦ��BaSO4������ˮ��Ҳ���������ᡣ
���������ۡ���������ˮ��pH��Χ�ǣ�7> pH> 5.6��ƫ���ԣ�������Ϊ �� ��
�������ܸ�ʴ������Ʒ���ӻ�����Ӧ�����Ͽ���Ҫ��Ӧ���� �� ��
���ռ���������Ʒ����һ��ʱ���pH��С��ԭ����SO2��ˮ��Ӧ���ɵ�H2SO3������ΪH2SO4����д���÷�Ӧ�Ļ�ѧ����ʽ �� ��
��������롿ͬѧ�ǶԸ��ռ�����������Ʒ�е����ʽ��в��룺
���������������ֻ����H2SO3��
���������������ֻ����H2SO4��
��������������� �� ��
��ʵ��̽����
��1������ռ���������Ʒ�еμӹ���Ba(OH)2��Һ���а�ɫ�������ɣ����ˡ�
������Һ�еμ� �� ��Һ����Һ�� �� ɫ��֤����������Ʒ�еμӵ�Ba(OH)2��Һ�ѹ�����
��������м����������ᣬ���������ܽ��ҷų��д̼�����ζ���塣�÷�Ӧ�Ļ�ѧ����ʽΪ �� �����������й����������ʵIJ��� �� ��ȷ��
��2��ijͬѧȡ������ƷV L������17.1%��Ba(OH)2��Һ�����ٲ�������ʱ��ǡ������10.00 g Ba(OH)2��Һ����V L������Ʒ���ܽ�SO2������Ϊ �� ��
��ʵ�鷴˼����ijЩ�����л��ɷ�������������ڣ��������ڿ����к���ijԪ��+4���������ԭ������������Ļ�ѧʽΪ �� ��
����չ���졿���ú�ˮ�����Ǽ���SO2�ŷŵ���Ч�������乤����������ͼ��ʾ��

��Ȼ��ˮ�����˽϶�ĺ�����������H2SO3���ɣ�H2SO3�뺣ˮ�е����ӷ�Ӧ�����ͷų�CO2��ͨ��������������ˮ������������ǿ��
�����һ�ּ��龻������������Ƿ�SO2�ļ�ʵ�鷽���� �� ��
��������ĺ�ˮ��Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ��ò�������ҪĿ���� �� ��
���������ۡ��ٿ����еĶ�����̼����ˮ������
���û���Ӧ ��2H2SO3 +O2="=" 2H2SO4
��������롿����H2SO3����H2SO4
��ʵ��̽������1���ٷ�̪ �죨��ʯ�� ���������������Լ��������������֣�
��BaCO3+2HCl��BaCl2+CO2��+H2O �����
��2��0.64 g
��ʵ�鷴˼��NO2
����չ���졿�ٽ������������ͨ��Ʒ����Һ������Һ��ɫ�����к�SO2����֮���ޡ�
���к͡�ϡ�;�����������ˮ�����ɵ��ᣨH+��
�⣺��������
��������ˮ��pH��Χ�ǣ�7��pH��5.6��ƫ���ԣ�������Ϊ�����еĶ�����̼����ˮ�����ԣ���������еĶ�����̼����ˮ�����ԣ�
�������ܸ�ʴ������Ʒ���ӻ�����Ӧ�����Ͽ���Ҫ��Ӧ�����û���Ӧ������û���Ӧ��
��SO2��ˮ��Ӧ���ɵ�H2SO3������ΪH2SO4���÷�Ӧ�Ļ�ѧ����ʽΪ��2H2SO3+O2�T2H2SO4��
��������롿
���������ʿ��ܼ���H2SO3����H2SO4���������H2SO3����H2SO4��
ʵ��̽��
��1��������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��֤����������Ʒ�еμӵ�Ba��OH��2��Һ�ѹ����������̪ �죮
��������м����������ᣬ���������ܽ��ҷų��д̼�����ζ���壮�÷�Ӧ�Ļ�ѧ����ʽΪ��BaSO3+2HCl=BaCl2+SO2��+H2O��
���������ܽ�˵�������м��������ᱵ���������ᱵ����������
��2����������������ΪX��
SO2+Ba��OH��2�TBaSO3+H20
64 171
X 10.00g��17.1%
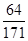 =
=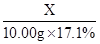
X=0.64g��
���0.64g��
ʵ�鷴˼
��������Ҳ���γ��������Ҫ���ʣ����������Ļ�ѧʽ��NO2�����NO2��
��չ����
�ټ��龻������������Ƿ�SO2��ʵ�鷽�����������������ͨ��Ʒ����Һ������Һ��ɫ�����к�SO2����֮���ޣ�����������������ͨ��Ʒ����Һ������Һ��ɫ�����к�SO2����֮���ޣ�
��������ĺ�ˮ��Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ��ò�������ҪĿ�����к͡�ϡ�;�����������ˮ�����ɵ��ᣮ����к͡�ϡ�;�����������ˮ�����ɵ���
��������ˮ��pH��Χ�ǣ�7��pH��5.6��ƫ���ԣ�������Ϊ�����еĶ�����̼����ˮ�����ԣ���������еĶ�����̼����ˮ�����ԣ�
�������ܸ�ʴ������Ʒ���ӻ�����Ӧ�����Ͽ���Ҫ��Ӧ�����û���Ӧ������û���Ӧ��
��SO2��ˮ��Ӧ���ɵ�H2SO3������ΪH2SO4���÷�Ӧ�Ļ�ѧ����ʽΪ��2H2SO3+O2�T2H2SO4��
��������롿
���������ʿ��ܼ���H2SO3����H2SO4���������H2SO3����H2SO4��
ʵ��̽��
��1��������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��֤����������Ʒ�еμӵ�Ba��OH��2��Һ�ѹ����������̪ �죮
��������м����������ᣬ���������ܽ��ҷų��д̼�����ζ���壮�÷�Ӧ�Ļ�ѧ����ʽΪ��BaSO3+2HCl=BaCl2+SO2��+H2O��
���������ܽ�˵�������м��������ᱵ���������ᱵ����������
��2����������������ΪX��
SO2+Ba��OH��2�TBaSO3+H20
64 171
X 10.00g��17.1%
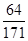 =
=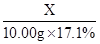
X=0.64g��
���0.64g��
ʵ�鷴˼
��������Ҳ���γ��������Ҫ���ʣ����������Ļ�ѧʽ��NO2�����NO2��
��չ����
�ټ��龻������������Ƿ�SO2��ʵ�鷽�����������������ͨ��Ʒ����Һ������Һ��ɫ�����к�SO2����֮���ޣ�����������������ͨ��Ʒ����Һ������Һ��ɫ�����к�SO2����֮���ޣ�
��������ĺ�ˮ��Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ��ò�������ҪĿ�����к͡�ϡ�;�����������ˮ�����ɵ��ᣮ����к͡�ϡ�;�����������ˮ�����ɵ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ

 2CO2+X�����С�X���Ļ�ѧʽΪ
2CO2+X�����С�X���Ļ�ѧʽΪ 