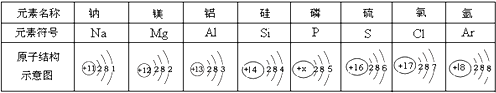
题目内容
【题目】化学基础与常识
(1)白开水容易解渴,促进新陈代谢,有调节体温、输送养分等功能。白开水是______(填“纯净物”或“混合物”)。
(2)开发和利用新能源是解决能源问题的重要途径.下列属于新能源的是__________(填字母序号).
A 潮汐能 B 太阳能 C 风能 D 石油.
(3)物质X是一种重要的阻燃剂.工业上用三氧化二锑(Sb2O3)生产X的化学方程式为:Sb2O3+2H2O2═X+2H2O.根据质量守恒定律,推断X的化学式为___________.
(4 )硫化氢(H2S)的回收是资源利用和环境保护的重要研究课题。将含H2S的废 气与空气混合,通入 FeCl3、FeCl2、CuCl2 的混合溶液回收硫(S),反应过程如图。
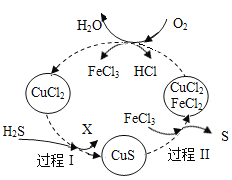
(Ⅰ)过程Ⅰ中 H2S 与 CuCl2 发生了复分解反应。写出该反应X 的化学方程式__________。
(Ⅱ)过程Ⅲ的反应物有__________
【答案】混合物 A、B、C Sb2O5 H2S+ CuCl2=CuS↓+2HCl HCl、FeCl2、O2
【解析】
(1)白开水是由水和其他可溶性杂质组成的,属于混合物;
(2)人们正在利用和开发的新能源有太阳能、核能、风能、地热能、潮汐能、生物质能等。故选ABC;
(3)根据质量守恒定律和方程式中的已知条件可得,反应前:2个Sb,7个O,4个H,反应后:4个H,2个O;比较反应前后原子的种类和个数可以判断在X中含有:2个Sb,5个O,即其化学式为:Sb2O5;
(4)(Ⅰ)H2S与CuCl2发生复分解反应生成硫化铜沉淀和盐酸,化学反应方程式为:H2S+CuCl2=CuS↓+2HCl;
(Ⅱ)过程Ⅲ中,氯化铜、氯化亚铁和氧气、氯化氢转化成氯化铁、水和氯化铜,所以反应物有:HCl、FeCl2、O2。

【题目】氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸HClO是一种弱酸.氯气溶于水所得溶液称为氯水.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.如图是实验室制取氯气的成套装置图,请填空:
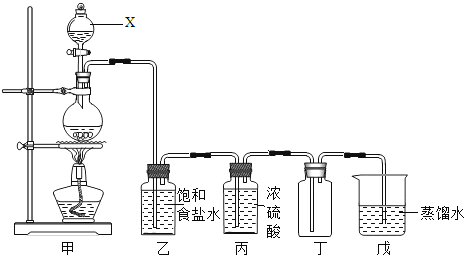
(1)仪器X的名称是:_____.
(2)从反应物的状态和反应条件看,装置甲属于_____型气体发生装置.
(3)氯气在装置丁中被收集,其收集方法为_____,装置戊中可得到氯水.
(4)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
(提出问题)氯水中的什么成分使品红试纸褪色?
(猜 想)猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;猜想4:氯水中的_____(填化学式)使品红试纸褪色.
(实验探究)
实 验 操 作 | 实 验 现 象 | 结 论 |
①把品红试纸放入水中 | _____ | 猜想1不成立 |
②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
③_____ | 试纸不褪色 | 猜想3不成立 |
(结 论)学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
(反 思)向氯水中滴加几滴紫色石蕊试液,会观察到的现象是_____.
【题目】化学兴趣小组在鲁老师的指导下进行课外探究实验,他们将剪断的火柴头置于酒精灯灯芯上,点燃酒精灯,意外的发现灯芯上的火柴头居然没烧着!这是什么原因呢?请你随他们一起探究。
【猜想与假设】猜想1:灯芯与焰心交界处温度低于火柴头的着火点。猜想2:灯芯与焰心交界处氧气浓度太低,不支持火柴头的燃烧。猜想3:两者均是影响因素。
【查阅资料】①火柴头主要由KClO3、MnO2、易燃物及粘合剂等组成,用红外线测温仪测得火柴头的着火点约是303.4℃。②火柴头在氧气浓度为12.2%的气体中不能燃烧。

【实验验证1】为了验证猜想1,小明利用高温传感器测定酒精灯灯芯和焰心交界处的温度(如图),得到的数据如下:
测量次数 | 第1次 | 第2次 | 第3次 |
温度/℃ | 236 | 243 | 240 |
(1)小明进行多次测量的目的是___________。
(2)仅由上表可知,灯芯上火柴头未烧着的原因是________________________。
(3)请写出火柴头擦燃过程中发生反应的化学方程式(根据资料提供物质)_______________,联想到火柴燃烧时出现的白烟,小明推测白烟的成分可能是______________。
【实验验证2】为了验证猜想2,小红用注射器抽取酒精灯灯芯和焰心交界处的气体,并利用氧气传感器测量氧气的体积分数,数据如表。
测量次数 | 第1次 | 第2次 | 第3次 | 平均值 |
氧气的浓度/% | 5.93 | 5.29 | 6.53 | 5.92 |
(4)根据实验1、2探究内容,可知猜想______________正确。
(5)小红测出的几组氧气浓度存在差异的原因可能是__________________。
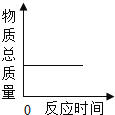
【反思评价】如图是小组同学将火柴头置于装有空气的密闭的容器中燃烧,并用氧气传感器在容器项端测量整个过程容器内氧气浓度变化,那么在_______________(填“A、B、C、D”)点时火柴头熄灭;

请你根据所学推理并解释曲线A8段、BC段、CD段氧气浓度变化的原因。①_____________________;②______________________;③_______________________。
【题目】松花蛋,又称皮蛋、变蛋。其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再放入鸭蛋浸渍。
请回答下列问题:
(1)生石灰加入沸水中,水能持续保持沸腾,其原因是_____。
(2)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为_____色。
(3)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动。
(提出问题)料液中含有哪些溶质?
(交流讨论)①一定含有NaOH、NaCl
②可能还含有其它溶质;
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是_____(用化学方程式表示)。
(实验探究)
实验步骤 | 实验现象 |
取少量上层料液,滴加过量_____ | 无明显现象 |
另取少量上层料液,滴加_____溶液 | 产生白色沉淀 |
(探究结论)_____同学的推断是正确的。