题目内容
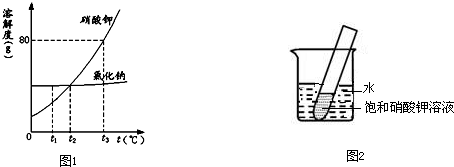
图1是氯化钠和硝酸钾两种物质的溶解度曲线,图2是氢氧化钙的溶解度曲线.根据图示回答下列问题.

(1)10℃时氯化钠的溶解度______(填“大于”“小于”或“等于”)硝酸钾的溶解度.将30℃时的硝酸钾饱和溶液转变为不饱和溶液的一种方法是______.从氯化钠溶液中结晶出氯化钠的方法是______.
(2)某同学从一瓶久置的氢氧化钙固体样品中取出0.2g,加入到30℃时100g水中,充分溶解后过滤,称得剩余固体0.08g.请你判断:滤液为______(填“饱和”或“不饱和”)溶液.
(3)将20℃时恰好饱和的硝酸钾溶液升温至60℃,一定没有变化的是______(填序号).
①水的质量 ②溶液中溶质的质量 ③溶质的质量分数 ④硝酸钾的溶解度.
解:(1)观察图表可以看出,10℃时氯化钠的溶解度大于硝酸钾的溶解度;因为硝酸钾的溶解度随温度的上升而增大,要使30℃时的硝酸钾饱和溶液转变为不饱和溶液,可以升高温度或增加溶剂;因氯化钠的溶解度受温度的影响不大,我们可以将溶液加热蒸发,使溶液达到饱和后,在蒸发掉溶剂,溶质就会结晶析出;
(2)从氢氧化钙的溶解度曲线图可以看出,30℃时,氢氧化钙的溶解度是0.15克,而现在100克水中溶解的氢氧化钙的质量是0.2克-0.08克=0.12克,故滤液为不饱和溶液;
(3)溶解度受温度的影响较大,升温后,溶解度变大;尽管硝酸钾的溶解度随着温度的升高而增大,但由于升温后溶液的组成可能不变,故溶质的质量、溶剂水的质量、溶液的质量可能不变,故溶液中溶质的质量分数可能不变.
故答案为:(1)大于;升温或加水;蒸发溶剂;(2)不饱和;(3)①②③.
分析:(1)观察图表分析;根据两种物质受温度影响的情况判断各自的方法;
(2)根据溶解度的概念联系图表综合分析判断;
(3)将20℃时的硝酸钾饱和溶液升温到60℃时,由于温度的升高,所以硝酸钾溶液的溶解度也会随着增大,但由于溶液的组成可能不发生改变,故溶质、溶液、溶质的质量分数均可能不变,而溶剂的质量不变.
点评:主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.
(2)从氢氧化钙的溶解度曲线图可以看出,30℃时,氢氧化钙的溶解度是0.15克,而现在100克水中溶解的氢氧化钙的质量是0.2克-0.08克=0.12克,故滤液为不饱和溶液;
(3)溶解度受温度的影响较大,升温后,溶解度变大;尽管硝酸钾的溶解度随着温度的升高而增大,但由于升温后溶液的组成可能不变,故溶质的质量、溶剂水的质量、溶液的质量可能不变,故溶液中溶质的质量分数可能不变.
故答案为:(1)大于;升温或加水;蒸发溶剂;(2)不饱和;(3)①②③.
分析:(1)观察图表分析;根据两种物质受温度影响的情况判断各自的方法;
(2)根据溶解度的概念联系图表综合分析判断;
(3)将20℃时的硝酸钾饱和溶液升温到60℃时,由于温度的升高,所以硝酸钾溶液的溶解度也会随着增大,但由于溶液的组成可能不发生改变,故溶质、溶液、溶质的质量分数均可能不变,而溶剂的质量不变.
点评:主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目