题目内容
(2011?东城区一模)为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示.当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%.试计算该样品中:(1)氯化钠的质量;
(2)碳酸钠的质量分数.
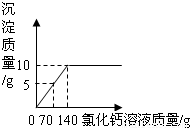
【答案】分析:(1)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得氯化钠的质量;
(2)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得碳酸钠的质量,进而求碳酸钠的质量分数.
解答:解:
设:样品中碳酸钠的质量为x,原混合物中的氯化钠的质量为y,生成氯化钠的质量为z.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g z
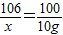
解得x=10.6g
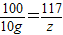
解得z=11.7g
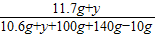 ×100%=6%
×100%=6%
解得y≈2.9g
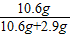 ×100%=78.5%
×100%=78.5%
答:样品中氯化钠的质量是2.9g;碳酸钠的质量分数是78.5%.
点评:考查根据化学方程式的计算及溶液质量分数的计算.
(2)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得碳酸钠的质量,进而求碳酸钠的质量分数.
解答:解:
设:样品中碳酸钠的质量为x,原混合物中的氯化钠的质量为y,生成氯化钠的质量为z.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g z
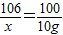
解得x=10.6g
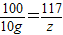
解得z=11.7g
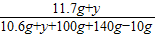 ×100%=6%
×100%=6%解得y≈2.9g
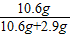 ×100%=78.5%
×100%=78.5%答:样品中氯化钠的质量是2.9g;碳酸钠的质量分数是78.5%.
点评:考查根据化学方程式的计算及溶液质量分数的计算.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
(2011?东城区一模)生活中离不开水.若水的硬度过大,会影响人体健康,因此需要进行软化处理.
(1)小文利用阳离子交换树脂对某硬水水样进行软化,其
原理示意如右图所示.树脂的作用是除去硬水中的______.
(2)生活中通过煮沸能够降低水的硬度.小文取此水样煮
沸后,发现有水垢生成.为探究水垢的成分,他进行了以下实验:
实验过程:
实验分析及结论:
①由实验Ⅰ可知,水垢分解的产物中一定有______.
②实验Ⅲ小试管内发生反应的化学方程式为______.
③根据实验探究,推测此水垢的成分中可能含有______.
(3)小文另取该水样,加入澄清石灰水,溶液变浑浊,其反应为:
A+Ca(OH)2═2CaCO3↓+2H2O,则A的化学式为______.
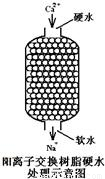
(1)小文利用阳离子交换树脂对某硬水水样进行软化,其
原理示意如右图所示.树脂的作用是除去硬水中的______.
(2)生活中通过煮沸能够降低水的硬度.小文取此水样煮
沸后,发现有水垢生成.为探究水垢的成分,他进行了以下实验:
实验过程:
| 实验序号 | 实验操作 | 实验现象 |
| Ⅰ |  | 水垢变白、变疏松, 澄清石灰水变浑浊 |
| Ⅱ |  | 固体部分溶解, 放出热量, 滤液的pH约为12 |
| Ⅲ |  | 实验现象是______. |
①由实验Ⅰ可知,水垢分解的产物中一定有______.
②实验Ⅲ小试管内发生反应的化学方程式为______.
③根据实验探究,推测此水垢的成分中可能含有______.
(3)小文另取该水样,加入澄清石灰水,溶液变浑浊,其反应为:
A+Ca(OH)2═2CaCO3↓+2H2O,则A的化学式为______.


