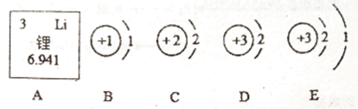题目内容
【题目】已知铜、铁均能与FeCl3溶液反应,![]() ,
,![]() 。现将铜、铁混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,有关烧杯中物质组成的说法正确的是( )
。现将铜、铁混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,有关烧杯中物质组成的说法正确的是( )
A.溶液中一定含有FeCl3,固定一定有Cu,可能有Fe
B.溶液中一定含有FeCl2,固体一定含Cu
C.溶液中一定含有FeCl2、CuCl2,固体一定含有Cu
D.溶液一定含有FeCl2,固体一定是Fe和Cu
【答案】B
【解析】
在金属活动性顺序中,铁位于铜之前,故将铜、铁混合粉末加入到盛有FeCl3溶液的烧杯中,铁先与氯化铁反应生成氯化亚铁,待铁完全反应后,铜再与氯化铁反应生成氯化亚铁和氯化铜。
A、由该过程发生的反应可知溶液中一定不含有氯化铁,因为反应后存在固体,不管该固体是哪种金属都不可能与氯化铁共存,从铁、铜的活动性可知反应时铁一定先参与反应,因此剩余固体中一定有铜,固体中是否含有铁,则要看铁的质量多少而定,不符合题意;
B、依据题干的信息可知铁、铜均能与氯化铁反应,所以溶液中一定含有氯化亚铁,从铁、铜的活动性可知反应时铁一定先参与反应,因此剩余固体中一定有铜,符合题意;
C、依据题干的信息可知铁、铜均能与氯化铁反应,所以溶液中一定含有氯化亚铁,如果氯化铁含量不足,铁能将其完全反应,铜未参与反应,则溶液中不含氯化铜,从铁、铜的活动性可知反应时铁一定先参与反应,因此剩余固体中一定有铜,不符合题意;
D、依据题干的信息可知铁、铜均能与氯化铁反应,所以溶液中一定含有氯化亚铁,从铁、铜的活动性可知反应时铁一定先参与反应,因此剩余固体中一定有铜,如果铁含量不足,氯化铁和铁完全反应后,再和铜反应,则固体中不含铁,不符合题意。
故选B。

【题目】某班学生在老师指导下探究铁与水蒸气的反应,请帮助他完成下列实验报告。
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是:_______
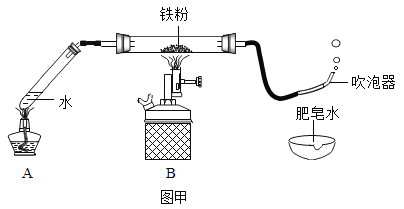
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
(查阅资料)铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没 有_____(填物质名称) |
取上述黑色固体少许,装入试管,加入足量硫酸铜溶液 | _____ ,有红色固体出现 | 黑色固体中一定 含有_____。 |
【题目】如图所示,在一只烧杯中进行实验。
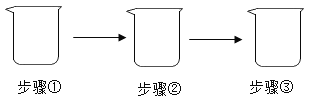
请补全实验方案
序号 | 目的 | 步骤 |
A | 检验NaCl中混有Na2CO3 | ①加入少量样品;②加入适量水至全部溶解; ③加入______ |
B | 验证NaCl不能无限溶解 | 20°C时①加入100g水;②加入10gNaCl; ③加入_____(已知:20℃时,NaCl的溶解度为36g) |
C | 配制_____ | 加入5gNaCl;②加入95g水;③搅拌至全部溶解 |