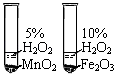题目内容
【题目】探究学习小组在实验室中用下图所示装置制取 CO2并探究CO2与过氧化钠(Na2O2)的反应. 
查阅资料得知:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2、H2O 发生反应:2Na2O2+2CO2═2Na2CO3+O2 , 2Na2O2+2H2O═4NaOH+O2↑.
请回答下列问题:
(1)装置A中发生反应的化学方程式为 , 利用装置 A 制取 CO2的优点是;
(2)装置B的作用是吸收CO2中混有的HCl,发生反应的化学方程式为;
(3)装置 D 的作用是;
(4)装置E中收集到的气体是(填化学式),该气体还可以用下图装置中的进行收集(填写字母序号); 
【答案】
(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;便于控制反应的发生和停止
(2)NaHCO3+HCl=NaCl+H2O+CO2↑
(3)除去二氧化碳气体
(4)O2;ad
【解析】解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,装置A可以通过压强的作用是固体和液体分离,所以利用装置A制取CO2的优点是:便于控制反应的发生和停止;(2)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,所以装置D的作用是除去二氧化碳气体;(4)过氧化钠和二氧化碳、水反应会生成氧气,氢氧化钠可以将二氧化碳除去,所以装置E中收集到的气体是O2,氧气密度比空气大,不易溶于水,密度比水小,所以还可以用下列图2装置中的ad进行收集.
所以答案是:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑,便于控制反应的发生和停止;(2)NaHCO3+HCl=NaCl+H2O+CO2↑;(3)除去二氧化碳气体;(4)O2,ad.
【考点精析】关于本题考查的书写化学方程式、文字表达式、电离方程式,需要了解注意:a、配平 b、条件 c、箭号才能得出正确答案.