题目内容
【题目】(5分)现将一定质量含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入溶质质量分数为10%的盐酸,生成气体的质量与加入盐酸的质量关系如图所示。
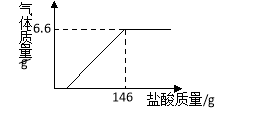
⑴当盐酸质量为150g时,溶液中溶质化学式为 ;
⑵求固体中碳酸钠的质量?(写出计算过程,保留一位小数)
⑶当充分反应后溶液中氯化钠的质量为g。
【答案】NaCl、HCl 15.9g ⑶23.4
【解析】
试题分析:将一定质量含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向其中加入稀盐酸,盐酸会和氢氧化钠先反应,然后再和碳酸钠反应,当盐酸质量为150g时,氢氧化钠和碳酸钠都已经被完全反应,所以溶质应该是生成的氯化钠和盐酸,化学式为NaCl、HCl,
设碳酸钠质量为x
Na2CO3 +2HCl ==2NaCl+H2O+CO2↑
10644106:44=x :6.6g x=15.9g
x 6.6g
当充分反应后溶液中氯化钠的的质量,可以分解氯元素守恒,总共消耗HCl的质量=146×10%=14.6,所以氯元素质量为14.6×35.5/36.5,设氯化钠质量为y,则35.5y/58.5=14.6×35.5/36.5,解得y=23.4g。

练习册系列答案
相关题目