题目内容
【题目】下图中A、B、C、D是四种粒子的结构示意图,E是银元素在元素周期表中的信息。请回答:

(1)图中A、B、C、D粒子共表示_____种元素;D中x =__________。
(2)A、B、C、D中表示的阳离子的离子符号为__________。
(3)一个银原子质量是一个碳12原子质量的____倍。
【答案】3 8 Al3+ 9
【解析】
(1)依据质子数不同元素种类不同,由图示可知四种微粒中共有质子数是13、17和18的三种元素;由于原子中质子数与核外电子数相等,观察可知该微粒的质子数是18,是具有稳定结构的氩原子,所以核外电子数也应为18,所以X为8;
(2)由四种粒子的结构示意图可知,在A中,核内质子数是13,核外电子数是10,是铝离子,离子符号为:Al3+;
(3)由元素周期表的信息可知,银的相对原子质量为108,由于相对原子质量之比等于其质量之比,所以一个银原子质量是一个碳12原子质量![]() 倍=9倍。
倍=9倍。

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
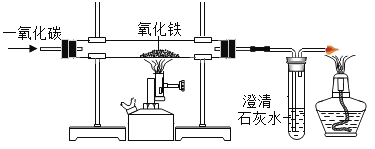
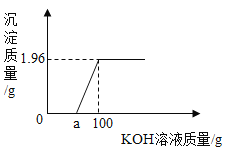
新卷王期末冲刺100分系列答案【题目】某化学实验室用稀硫酸处理含有氢氧化钠的废水。现取废水样品80g倒入烧杯中,加入几滴无色酚酞溶液,然后逐滴加入9.8%的稀硫酸,反应过程中溶液的pH变化如图所示。

(1)当恰好完全反应时,溶液的颜色变化是____________。
(2)求废水中氢氧化钠的质量分数_______ (写出计算过程)。
(3)往上述80g废水中逐渐加入稀硫酸至过量,请在答题卡中画出Na2SO4质量随加入稀硫酸质量变化的曲线_______。
(4)下表为市面上浓硫酸和浓盐酸的有关数据:
物质 | 纯度 | 价格(元/kg) |
浓硫酸(工业级) | 98% | 0.6 |
浓盐酸(工业级) | 98% | 0.4 |
若工厂每天需处理上述废水8吨,选用__________(填“浓硫酸”或“浓盐酸”)更合算,每天可节约________元(保留整数)。
【题目】化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧化钠溶液的反应进行了探究:
(1)探究稀盐酸与氢氧化钠溶液发生了反应,同学们设计了实验方案一:
实验步骤 | 实验现象 | 结论 |
取少量稀盐酸,先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液,并不断振荡,同时测定混合液的pH. | pH逐渐变大至pH=7,最后pH>7 | 稀盐酸与氢氧化钠溶液能发生反应 |
①请你分析上述方案中为什么强调只有测得的pH=7,最后pH>7才能证明反应发生了?______。
②写出稀盐酸与氢氧化钠溶液反应的化学方程式______。
(2)探究稀盐酸与氢氧化钠溶液反应是放热的,同学们设计了实验方案二:
取20℃时的NaOH溶液10mL于烧杯中,逐滴滴入稀盐酸,然后用温度计测量溶液温度。随着盐酸的加入,烧杯中溶液温度与加入盐酸体积之间的变化关系如图一所示:

①滴加至8mL时,充分搅拌后滴入紫色石蕊试液,溶液呈______色,盐酸滴加至______mL时,溶液呈中性。
②继续滴加盐酸,溶液的温度下降的原因是______。是否可以用NaOH固体代替氢氧化钠溶液探究中和反应是否放热?______(填“是”或“否”)。
(3)小强同学对方案二的实验有异议,他找到了前几天所做的实验数据记,图二是烧杯中溶液温度与加入盐酸体积之间的变化关系图,造成两位同学所测溶液温度有差异的原因可能是:①______,②______。