题目内容
将一定量的锌粉加入Cu(NO3)2和AgNO3的混合液中,充分反应后过滤,得到蓝色滤液和滤渣,下列有关分析错误的是( )
| A、滤液中一定有入Zn(NO3)2和Cu(NO3)2 |
| B、滤渣中一定有Ag和Cu |
| C、滤液中可能含有AgNO3 |
| D、可加入HCl确定滤液成分 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据金属活动性由强到弱的关系(Zn>Cu>Ag),锌可置换硝酸银中的银、锌可置换硝酸铜中的铜,生成的铜还可以置换硝酸银中的银,充分反应后得到蓝色滤液和滤渣,说明了滤液中有硝酸铜,锌全部参加了反应,根据以上反应及现象,分析反应的发生情况,推断所得固体及溶液中的离子.
解答:解:由题意可知,向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,发生的反应有锌可置换硝酸银中的银、锌可置换硝酸铜中的铜,生成的铜还可以置换硝酸银中的银,充分反应后得到蓝色滤液和滤渣,说明了滤液中有硝酸铜,锌全部参加了反应,锌没有剩余,由此可知:
A、锌和硝酸银发生了置换反应,溶液显蓝色,则滤液中一定有Zn(NO3)2和Cu(NO3)2,故A正确;
B、锌可能和硝酸铜发生了反应,没有置换完,也可能没有参与置换反应,所以滤渣中一定有Ag,可能含有Cu,故B错误;
C、锌的量比较少,可能只反应了少量的硝酸银,所以滤液中可能含有AgNO3,故C正确;
D、盐酸和硝酸银会发生反应生成氯化银沉淀,所以可加入HCl确定滤液成分,故D正确.
故选:B.
A、锌和硝酸银发生了置换反应,溶液显蓝色,则滤液中一定有Zn(NO3)2和Cu(NO3)2,故A正确;
B、锌可能和硝酸铜发生了反应,没有置换完,也可能没有参与置换反应,所以滤渣中一定有Ag,可能含有Cu,故B错误;
C、锌的量比较少,可能只反应了少量的硝酸银,所以滤液中可能含有AgNO3,故C正确;
D、盐酸和硝酸银会发生反应生成氯化银沉淀,所以可加入HCl确定滤液成分,故D正确.
故选:B.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
下列实验现象的描述正确的是( )
| A、硫在氧气里燃烧,发出蓝紫色火焰 |
| B、红磷燃烧产生大量白雾 |
| C、碳在氧气里燃烧,发出蓝色火焰 |
| D、铁丝在氧气中燃烧,火星四射,吸收热量 |
某纯净物A在纯净的氧气中燃烧:A+O2→H2O+CO2,可推知A物质( )
| A、是单质碳 |
| B、只含有碳元素和氢元素 |
| C、一定含有碳、氢、氧三种元素 |
| D、一定含有碳、氢二种元素,可能含有氧元素 |
要使硝酸钾的溶解度增大,可采用的措施是( )
| A、加硝酸钾 | B、升高温度 |
| C、快速搅拌 | D、蒸发水分 |
下列化学现象描述不正确的是( )
| A、把盛有硫的燃烧匙伸进充满氧气的集气瓶中,硫立即燃烧 |
| B、硫在空气里燃烧发出微弱的淡蓝色火焰,生成一种有刺激性气味的气体 |
| C、硫在氧气里燃烧发出明亮的蓝紫色火焰,生成一种有刺激性气味的气体 |
| D、铝箔在氧气里剧烈燃烧,发出耀眼的白光,生成一种白色固体 |
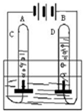 水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.
水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.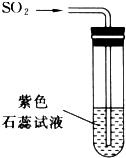 已知常温下二氧化硫是无色气体,它能与水反应生成亚硫酸:
已知常温下二氧化硫是无色气体,它能与水反应生成亚硫酸: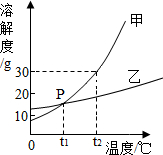 甲、乙两物质溶解度曲线如图所示.
甲、乙两物质溶解度曲线如图所示.