题目内容
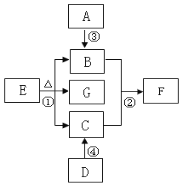
【题目】美国普度大学研发出一种利用铝镓合金制备氢气的新工艺,流程如下图所示。下列叙述正确的是
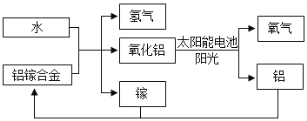
A. 氧化铝制得铝的反应中,铝元素的化合价不变
B. 流程中氧化铝、水、氧气都属于氧化物
C. 铝镓合金可以循环使用
D. 氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的反应类型是分解反应
【答案】CD
【解析】
A、氧化铝中,铝元素的化合价为+3价,单质铝的化合价为0价,故由氧化铝制得铝的反应中,铝元素的化合价改变,选项错误;
B、流程中的氧化铝、水都是由两种元素组成且含有氧元素的化合物,属于氧化物,而氧气属于单质,选项错误;
C、观察流程图发现开始的反应物是铝镓合金,最终的生成物是铝镓合金,所以铝镓合金能循环使用,选项正确;
D、氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应符合“一变多”的形式,属于分解反应,选项正确。故选CD。

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】某研究小组在学习氧气的化学性质时发现,铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰,该小组进行如下的探究:
(1)写出铁丝燃烧的文字表达式:__________
(2)探究 一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生如图所示);
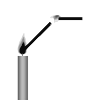
由此可知:蜡烛燃烧产生的火焰是由_______(填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 沸点/℃ | 燃烧时的温度/℃ | 是否有火焰 |
石蜡 | 300~550 | 约600 | 有 |
硫 | 444 | 暂无数据 | 有 |
铁 | 2750 | 约1800 | 无 |
钠 | 883 | 约1400 | 待测 |
①通过分析上表的数据,你认为物质燃烧时,什么情况下能产生火焰: ______;
②请推测金属钠在燃烧时________(填“有”或“无”)火焰产生
③表中硫的燃烧时温度是“暂无数据”,你认为合理的是___________(填编号)
A、200 B、300 C、400 D、800
【题目】某化学兴趣小组回收废旧干电池填料中的二氧化锰和氯化铵.
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如下图所示.
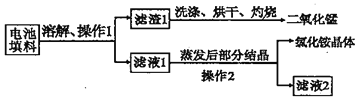
(1)操作 1 的名称是______,该操作中玻璃棒的作用是______.
(2)灼烧滤渣 l 的目的是________.
(3)二氧化锰是氯酸钾受热分解的催化剂,下表是他们的有关实验数据,请你回答有关问题:
二氧化锰与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
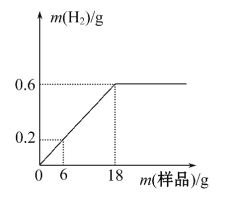
据上表可知二氧化锰与氯酸钾的质量比为____时,反应速率最快.分析可知反应前后二氧化锰在固体混合物中质量分数是____(选填“不变”或“变大”或“变小”).
【题目】某某学习小组的同学对过氧化氢分解进行探究。
Ⅰ.(探究一)影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
实验序号 | H2O2溶液的溶质质量分数% | 温度℃ | MnO2粉末用量/g | 反应时间 |
① | 30 | 35 | 0 | t1 |
② | 30 | 55 | 0 | t2 |
③ | 5 | 20 | 0.1 | 3s |
④ | 15 | 20 | 0.1 | 1s |
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1______t2(填“>”“=”“<”)
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是_____(填实验序号),合理的结论是__________。
(交流探讨)MnO2属于金属氧化物,其它金属氧化物能否起到类似MnO2的催化作用?
Ⅱ、(探究二)探究Fe2O3是否对过氧化氢分解起催化作用
操作步骤 | 实验情况记录 | 结论 | |
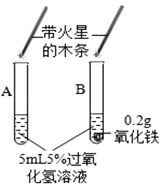
① |
| A试管上方带火星的木条未复燃 B中出现气泡快,带火星的木条复燃 | Fe2O3_____(填“不影响”、“减慢”或“加快”)过氧化氢分解 |
② | 将B试管中的混合物过滤,把滤渣烘干、_____。 | 固体质量0.2g | Fe2O3质量未变 |
小组的同学认为要证明Fe2O3是催化剂,上述二个实验还不够,还需要再增加一个实验,
a、该实验的目的是:____________
b、请你设计实验证明,简要的写出实验步骤及实验现象:_________。
(得出结论)过氧化氢分解快慢受温度、浓度、催化剂等因素影响。