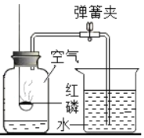
题目内容
【题目】请你根据所学化学基础知识与常识填空:
(1)下图是金属应用的实例,主要利用金属的导热性的是______(填序号);




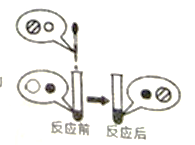
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如右图所示(其中![]() 表示不同离子)。则
表示不同离子)。则![]() 与
与![]() 反应生成了______(填物质名称);
反应生成了______(填物质名称);
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:![]() ,则X的化学式为______;
,则X的化学式为______;
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示: (碘的化学式为![]() )
)
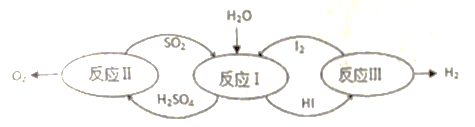
写出反应1中发生反应的化学方程式______。
【答案】B 水 CaF2 SO2+I2+2H2O=H2SO4+2HI
【解析】
(1)A中电缆是利用了金属的导电性,故不符合题意;B中电热壶主要是利用电热丝的导热性,故符合题意;C中金属丝是利用了金属的延展性,故不符合题意;D中金属乐器是利用了金属可以传导声音的性质,同时,将金属制作成金属乐器也是利用了金属的延展性,故不符合题意。故选:B。
(2)氢氧化钠溶液中存在钠离子和氢氧根离子,稀盐酸中存在氢离子和氯离子,氢氧化钠与稀盐酸反应生成氯化钠和水,氯化钠在水中以钠离子和氯离子的形式存在,故水中依然存在钠离子和氯离子,由图示可知,![]() 与
与![]() 反应生成了水。故填:水。
反应生成了水。故填:水。
(3)根据化学方程式中的质量守恒定律可知,方程式左边有一个钙原子右边没有,左边有六个氟原子右边只有四个,左边有六个氢原子三个氧原子与右边相等,所以X中含一个钙原子和两个氟原子, X的化学式为CaF2。故填:CaF2。
(4)由图示可知,反应Ⅰ的反应物有SO2、I2和H2O,产物有H2SO4和HI,将反应物和产物写在等号两边再配平可得反应Ⅰ的化学方程式。故填:SO2+I2+2H2O=H2SO4+2HI。

 名校课堂系列答案
名校课堂系列答案