题目内容
用海水制得的粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。请回答下列问题:
(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、 、计算产率;
(2)若要去除粗盐中可溶性的杂质氯化镁和氯化钙,可以依次加入过量的氢氧化钠和碳酸钠两种溶液,写出其中的一个化学方程式 ,过滤后向滤液中加入过量的盐酸,其目的是 ,最后通过蒸发结晶得到较为纯净的氯化钠。
(1)蒸发;(2) MgCl2+2NaOH=Mg(OH)2↓+2NaCl(或Na2CO3+ CaCl2 =CaCO3↓+2NaCl) 除去多余的氢氧化钠和碳酸钠
解析

下图表示实验室用稀H2SO4、CuO、Fe粉三种物质,制取铜的两种实验方案。
|
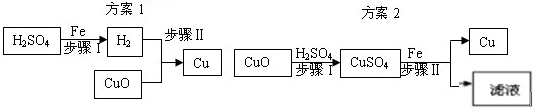 (1)若按方案1制取铜,步骤II反应的现象是 。
(1)若按方案1制取铜,步骤II反应的现象是 。(2)若按方案2制取铜,步骤I发生反应的化学方程式 。
(3)两种方案比较,方案 更好,理由是: 。
小明发现家中施用的碳酸氢铵(NH4HCO3)减少了,并闻到一股刺激性的气味。他很好奇,于是和同学们进行探究,请你一同参与:
[提出问题] 碳酸氢氨减少的原因是什么?
[猜想假设] 碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
[实验设计] 小明设计了如图所示的装置进行实验 (实验装置中的铁架台省略)。
(1)A装置大烧杯中的生石灰和水的作用是 。
(2)装置B中澄清石灰水 ,证明产物中有二氧化碳生成。
(3)根据现象 ,证明实验后生成了水和氨气。
(4)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再经过某实验操作,也可以证明碳酸氢铵分解后有二氧化碳生成,请你帮她设计完成实验:
| 实验步骤 | 实验现象 | 反应的方程式 |
| | | |
[实验结论]碳酸氢铵受热易分解,其反应的化学方程式为 。
[实验反思]根据以上实验,你认为是 ,在施用时注意 。
实验室利用H2+CuO Cu+H2O反应原理(实验装置见下图),测定水分子中氢氧原子的“相对原子质量”比值,实验室中制得的氢气中有少量水蒸气。则有关实验操作说法正确的是
Cu+H2O反应原理(实验装置见下图),测定水分子中氢氧原子的“相对原子质量”比值,实验室中制得的氢气中有少量水蒸气。则有关实验操作说法正确的是
| A.只需要获得氧化铜粉前后的质量差 |
| B.只需要获得无水硫酸铜前后的质量差 |
| C.若没有“甲”装置,所得比值偏大 |
| D.实验中一定要通入足量的氢气将氧化铜完全反应 |



