题目内容
【题目】利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,其制取的主要流程如图所示(反应条件已略去):

已知:2Cu+2H2SO4+O2=2CuSO4+2H2O。
(1)过程Ⅱ中分离操作的名称是_____________;该操作需要用到的玻璃仪器有烧杯玻璃棒和________,其中玻璃棒的作用是________________________。
(2)过程Ⅲ中有气体产生,反应的化学方程式为:_____________________。
(3)A-E中含铜、锌两种元素的物质有_____(填字母)。
【答案】过滤 漏斗 引流 Zn+HSO4=ZnSO4+H2↑ AC
【解析】
由题意可知,含Cu、Zn铜帽与稀硫酸和氧气反应生成了硫酸铜和硫酸锌的混合液A,根据实验的目的,为了得到铜和硫酸锌,应向A溶液加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应加入稀硫酸D,据此分析解答。
(1)过程Ⅱ中为了分离固体和液体,操作的名称是过滤;该操作需要用到的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流;
(2)过程Ⅲ中是稀硫酸与锌反应生成了硫酸锌和氢气,反应的方程式是:Zn+H2SO4=ZnSO4+H2↑;
(3)由上述分析可知,溶液A是硫酸铜和硫酸锌的混合物,固体C是铜和锌的混合物。所以,含铜、锌两种元素的物质有AC。

 学习实践园地系列答案
学习实践园地系列答案【题目】某兴趣小组通过镁与稀盐酸反应探究影响反应速率的因素(镁的质量相等,镁条的形状一样,稀盐酸均过量),设计实验如表:
实验编号 | 盐酸的质量分数 | 镁的形态 | 溶液初始温度/℃ |
① | 3% | 粉末 | 30 |
② | 3% | 条状 | 20 |
③ | 6% | 粉末 | 20 |
④ | 6% | 条状 | 20 |
(1)镁与稀盐酸反应的化学方程式为______。
(2)若四组实验均以收集到250mL氢气为标准,要比较各组反应速率,则以上实验还需要测出的数据是______。
(3)实验______和______(填实验编号)是研究盐酸的浓度对该反应速率的影响。
(4)测定在不同时间产生的氢气的体积数据,绘制出图1,则实验②对应的曲线可能是______(填序号)。
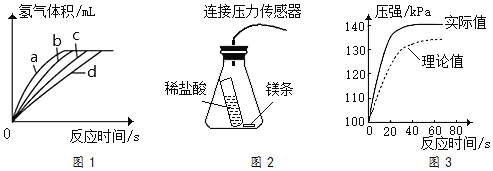
(5)利用图2压力传感器进行实验,得到图3锥形瓶内的压强随时间变化的曲线图,发现实验测得的实际值比理论值偏大。请分析可能的原因______。
【题目】归纳与反思是学习化学的重要环节。下列各项归纳完全正确的是![]()
![]()
|
|
氧气有助燃性:用作燃料 增加粮食产量:施用过量化肥、农药 一氧化碳有还原性:用于冶炼金属 | 核电荷数最小的原子:H 地壳中含量最高的金属元素:铁 天然存在的最硬的物质:金刚石 |
|
|
鉴别软水和硬水:肥皂水 除去冰箱中的异味:活性炭吸附 生活中使用乙醇汽油:无污染 | 氧气:由氧气分子构成 金属铜:由铜原子构成 氯化钠:由 |
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()