题目内容
60
℃时,将36g硝酸钾溶于204g水中,其溶质质量分数为______.将此溶液平均分成三份:(1)
取第一份溶液,将温度升高至90℃(不考虑水分蒸发),所得溶液的溶质质量分数为______;(2)
取第二份溶液,将其溶质质量分数增大一倍,需加入固体______g;(3)
取第三份溶液,使其质量分数变为原来的一半,需加入_____g水.
答案:15%;15%;17.1;80
解析:
提示:
解析:
|
解析:所配溶液的溶质质量分数为 36g/(36g+204g)×100%=15%,平均分成三份后,每一份溶液的质量为80g,含溶质的质量为12g,溶质质量分数为15%.(1)升温后,溶质和溶剂的质量都不变,故溶质质量分数仍为15%;(2)溶质质量分数增大一倍,即变为30%,设加入固体的质量为x,则(12+x)×100%/(80+x)=30%x=17.1g;(3)溶质质量分数变为原来的一半,即变为7.5%,设需要加入水的质量为y,则12g/(80g+y)=7.5% y=80g |
提示:
|
点拨:无论是改变溶质的质量还是改变溶剂的质量,都会引起溶液质量的改变. |

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下表是KNO3、NaCl在不同温度下的溶解度。
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
245 |
|
NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |
(1)依据上表数据,绘制KNO3、NaCl的溶解度曲线,下图1中能表示KNO3溶解度曲线的是_________________。(填“a”或“b”)
(2)下图1中P点的含义是__________________________________。
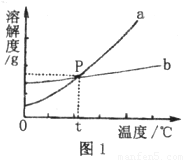
(3)欲使硝酸钾不饱和溶液转化为饱和溶液,可以采取的方法之一是_______________。
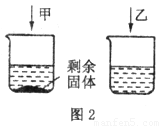
(4)30℃时,在两个各盛有100g水的烧杯中,分别加入相同质量的氯化钠和硝酸钾,充分溶解后,其结果如上图2所示,加入的甲物质是_________________。
(5)硝酸钾中含有少量氯化钠时,可通过_________________(填“蒸发结晶”或“降温结晶”)的方法提纯。
(6)20℃时,136g饱和食盐水,蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为________g。
(7)60℃时,将60g硝酸钾放入盛有50g水的烧杯中,充分搅拌,所得溶液的质量为________g。