题目内容
高纯硅是制造计算机电路芯片的主要原料.请回答:
(1)地壳中 元素的含量仅次于硅元素.
(2)工业上用石英(主要成分为SiO2)制备粗硅的反应为:SiO2+2C
Si+2R↑,二氧化硅中硅元素的化合价为 ,生成物R的化学式为 .
(3)硅在氧气中燃烧生成二氧化硅,并放出大量的热,可作未来新能源,其反应方程式为 .
(1)地壳中
(2)工业上用石英(主要成分为SiO2)制备粗硅的反应为:SiO2+2C
| ||
(3)硅在氧气中燃烧生成二氧化硅,并放出大量的热,可作未来新能源,其反应方程式为
考点:地壳中元素的分布与含量,有关元素化合价的计算,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:物质的微观构成与物质的宏观组成,化学用语和质量守恒定律
分析:(1)地壳中元素含量由多到少的前四位元素为氧、硅、铝、铁;
(2)根据化学变化前后原子种类不变、原子数目没有增减,由反应的化学方程式推断生成物R的分子构成及化学式;
(3)根据题中对反应的描述,判断反应的反应物与生成物,从而完成反应化学方程式的书写.
(2)根据化学变化前后原子种类不变、原子数目没有增减,由反应的化学方程式推断生成物R的分子构成及化学式;
(3)根据题中对反应的描述,判断反应的反应物与生成物,从而完成反应化学方程式的书写.
解答:解:(1)地壳中含量最多的元素为氧元素,其次是硅元素;
故答案为:氧(或O);
(2)氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
根据反应的化学方程式SiO2+2C
Si+2R↑,反应前Si、O、C三种元素的原子个数依次为1、2、2,而反应后Si、O、C三种元素的原子个数依次为1、0、0,所以在物质R的2个分子中应含有2个O原子和2个C原子,则每个R分子由1个C原子和1个O原子构成;则物质R的化学式为CO;
故答案为:+4;CO;
(3)硅在氧气中燃烧生成二氧化硅,即在点燃条件下,硅与氧气反应生成二氧化硅;
故答案为:Si+O2
SiO2.
故答案为:氧(或O);
(2)氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
根据反应的化学方程式SiO2+2C
| ||
故答案为:+4;CO;
(3)硅在氧气中燃烧生成二氧化硅,即在点燃条件下,硅与氧气反应生成二氧化硅;
故答案为:Si+O2
| ||
点评:物质的化学式可以表示物质的组成也可以表示该物质的一个分子的构成,根据物质的化学式可推断物质的分子构成,根据分子的构成也可写出物质的化学式.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
“洁厕灵”与“漂白精”不能混用,二者若混合易产生一种有毒气体,反应的化学方程式为:NaClO+2HCl═NaCl+x↑+H2O,则X的化学式为( )
| A、C12 |
| B、O3 |
| C、O2 |
| D、H2O |
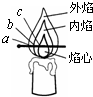 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.