题目内容
【题目】将16g高锰酸钾放在试管里加热,过一段时间后,撤去了酒精灯,称得剩余固体的质量是14.4g。求剩余固体中各成分的质量。
【答案】高锰酸钾0.2g;锰酸钾9.85g;二氧化锰4.35g
【解析】本题考查的根据关化学方程式的计算,通过认真分析题文,根据质量守恒定律得到氧气的质量是解题的关键。
由题意可以知道,生成氧气的质量为16g-14.4g=1.6g
设生成K2MnO4的质量为x,MnO2的质量为y
2KMnO4△ K2MnO4+MnO2+O2↑
197 87 32
x y 1.6g
![]()
![]()
解得:x=9.85g y=4.35g
根据质量守恒定律可以知道反应消耗高锰酸钾的质量为:9.85g+4.35g+1.6g=15.8g
所以没有反应的高锰酸钾的质量为:16g-15.8g=0.2g
答:剩余固体物质中含有高锰酸钾0.2g,锰酸钾9.85g,二氧化锰4.35g。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】某同学用如下装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去)。
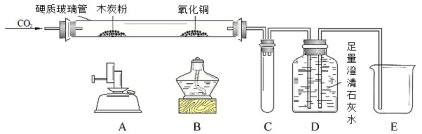
在完成气密性检查后加入药品,并已设法在装置中充满二氧化碳。
实验步骤 | 实验现象 | 实验分析 |
①缓缓通入CO2,点燃A处酒精喷灯,一段时间。 | 木炭粉减少,D中有气泡、石灰水变浑浊且 (1) 。 | 硬质玻璃管中发生反应的化学方程式为 (2) 。 |
②点燃B处酒精灯,一段时间。 | B处玻璃管内 (3) 。 | 以上实验说明 (4) 具有还原性。 |
③停止通入二氧化碳,熄灭A、B两处火焰。 | C中 (5) 。 |
有同学认为该装置需要添加尾气处理装置,你认为是否需要并说明理由 (6) 。