题目内容
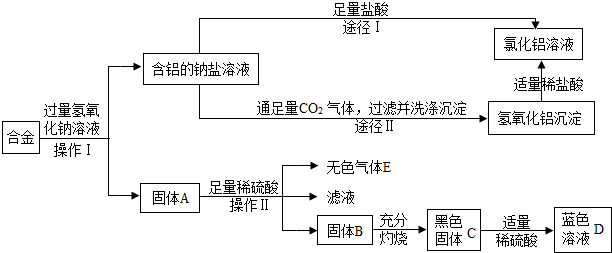
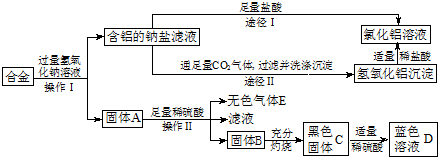
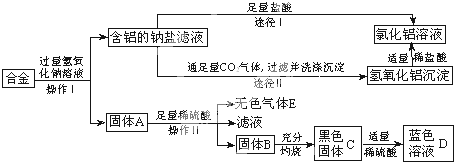
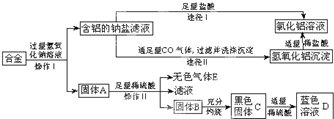
(9分)兴趣小组的同学在开展“废物利用、减少污染”的活动中,取某工厂合金废料(含铝、铁、铜)进行如下实验:
(1)操作Ⅰ的名称是 ;该操作需用到的铁制仪器为 。
(2)固体A的成分是 ;操作Ⅱ反应的化学方程式为 。
(3)黑色固体C加适量稀硫酸反应的方程式为 。
(4)图中由含铝的钠盐制备氯化铝有两种途径,你认为合理的途径是 (填:“Ⅰ”或“Ⅱ”),理由是 。
(1)、 过滤 、 铁架台
(2)、 铁、铜 、 H2SO4+Fe==FeSO4+H2↑
(3)CuO+H2SO4==CuSO4+H2O
(4)、 Ⅱ 、 不含杂质
解析试题分析:根据图示的转化情况分析。
(1)由于操作I是分离固体与液体的操作,故应该是过滤,则所用到的铁制仪器有铁架台或三脚架。
(2)根据D是蓝色溶液,可知溶液中含有铜离子,而D是由黑色固体C和稀硫酸反应制得,则可知黑色固体C应是氧化铜;而固体B充分灼烧后可生成C(氧化铜),故可知固体B是单质的铜。而根据图示的转化情况分析可知,合金废料中的铝能和足量的氢氧化钠溶液反应生成含铝的钠盐,则固体A中一定含有铁和铜,其中铁能与稀硫酸反应生成氢气E,即H2SO4+Fe=FeSO4+H2↑,而铜不反应,则过滤得到固体B,符合题意。
(3)氧化铜与硫酸反应生成硫酸铜与水,故反应的化学方程式为CuO+H2SO4=CuSO4+H2O;
(4)由于途径I在反应过程中没有去除钠盐,且加入了足量的盐酸来反应,所以制备的氯化铝中会含有钠盐和剩余的盐酸;而途径II是通过先得到纯净的氢氧化铝沉淀,再与适量的盐酸完全反应后制得氯化铝,会更纯净些。
考点:过滤的原理、方法及其应用,金属的化学性质,酸的化学性质,书写化学方程式,化学实验方案设计与评价
点评:熟练掌握一些特殊反应的特殊现象及特殊物质的特殊性质或应用,对于与本题相似的推断类题的解决会起到关键作用。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案