题目内容
(2011?抚顺)化学课上,老师拿出一个包装袋,上面写着“食品保鲜剂”,让同学们对它的成分进行探究.
老师为同学们提供了如下信息:
(1)食品保鲜剂是利用它的有效成分能吸收空气中氧气或水蒸气来防止食品腐败的.
(2)此袋保鲜剂的有效成分是以下四种物质中的一种:
①生石灰 ②氢氧化钠固体 ③铁粉 ④浓硫酸
[初步探究]
(1)同学们经过讨论,一致认为上述四种物质中的氢氧化钠固体和浓硫酸都不适合做食品保鲜剂,理由是
(2)同学们打开保鲜剂的包装,观察到包装袋内的物质为白色固体,则该保鲜剂的有效成分一定不是
[实验探究]
同学们对该袋物质的成分进行了如下研究,请你帮他们完成实验报告.
[拓展应用]
同学们还发现,有的食品采用充气包装的保鲜,对所充气体的基本要求为:
①无毒;②
请你写出一种可以填充到食品包装内的气体
老师为同学们提供了如下信息:
(1)食品保鲜剂是利用它的有效成分能吸收空气中氧气或水蒸气来防止食品腐败的.
(2)此袋保鲜剂的有效成分是以下四种物质中的一种:
①生石灰 ②氢氧化钠固体 ③铁粉 ④浓硫酸
[初步探究]
(1)同学们经过讨论,一致认为上述四种物质中的氢氧化钠固体和浓硫酸都不适合做食品保鲜剂,理由是
氢氧化钠和浓硫酸都具有很强的腐蚀性
氢氧化钠和浓硫酸都具有很强的腐蚀性
.(2)同学们打开保鲜剂的包装,观察到包装袋内的物质为白色固体,则该保鲜剂的有效成分一定不是
③(或Fe或铁粉)
③(或Fe或铁粉)
.[实验探究]
同学们对该袋物质的成分进行了如下研究,请你帮他们完成实验报告.
| 实验步骤 | 实验现象 | 结论与解释 | |
| 步骤1:取少量样品于试管中,加入适量的水振荡 | 形成白色浑浊液体,用手触摸试管外壁感到发热 | 该样品中一定含有 的物质 ①生石灰(或 CaO或氧化钙) ①生石灰(或 CaO或氧化钙) 发生反应的化学方程式: CaO+H2O=Ca(OH)2 CaO+H2O=Ca(OH)2 | |
| 步骤2:过滤步骤1中所得浑浊液体,将滤渣和滤液分别放入两支试管中 | 向盛有滤渣的试管中加入足量的稀盐酸 | 白色固体消失,有气泡产生 | 该样品中还一定含有的物质是 碳酸钙(或CaCO3) 碳酸钙(或CaCO3) |
| 向盛有滤液的试管中通入二氧化碳气体 | 溶液变浑浊 | 不能确定的物质是 氢氧化钙(或熟石灰 或Ca(OH)2) 氢氧化钙(或熟石灰 .或Ca(OH)2) | |
同学们还发现,有的食品采用充气包装的保鲜,对所充气体的基本要求为:
①无毒;②
不与食品发生化学反应(或化学性质稳定)
不与食品发生化学反应(或化学性质稳定)
;③廉价易获得.请你写出一种可以填充到食品包装内的气体
氮气(或N2、二氧化碳或CO2)
氮气(或N2、二氧化碳或CO2)
.分析:作食品保鲜剂的物质必须无毒、无害、无腐蚀性,因为氢氧化钠和浓硫酸都具有很强的腐蚀性,所以氢氧化钠固体和浓硫酸都不适合做食品保鲜剂;保鲜剂为白色,而铁粉是黑色的,因此一定不是铁粉;所以保鲜剂只可能是氧化钙.
解答:解:(1)根据作食品保鲜剂的物质必须无毒、无害、无腐蚀性,因为氢氧化钠和浓硫酸都具有很强的腐蚀性,所以氢氧化钠固体和浓硫酸都不适合做食品保鲜剂;
(2)保鲜剂袋内的物质为白色固体,而铁粉是黑色的,因此保鲜剂一定不是铁粉;只可能是生石灰;
与水反应的化学方程式为:CaO+H2O=Ca(OH)2 ;
根据碳酸钙遇盐酸放出气体,滤渣的试管中加入足量的稀盐酸,白色固体消失,有气泡产生,因此样品中还一定含有的物质是碳酸钙(或CaCO3);
向盛有滤液即氢氧化钙溶液的试管中通入二氧化碳气体,变浑浊,不能确定的物质是氢氧化钙(或熟石灰或Ca(OH)2)
[拓展应用]
充气包装的保鲜,对所充气体的基本要求为:无毒、无味、无嗅,化学性质稳定,廉价易获得;可以填充到食品包装内的气体如:氮气、二氧化碳;
故答案为:(1)氢氧化钠和浓硫酸都具有很强的腐蚀性;
(2)③(或Fe或铁粉);①生石灰(或CaO或氧化钙);CaO+H2O=Ca(OH)2 ;碳酸钙(或CaCO3);
氢氧化钙(或熟石灰或Ca(OH)2);
[拓展应用]
不与食品发生化学反应(或化学性质稳定);氮气(或N2、二氧化碳或CO2).
(2)保鲜剂袋内的物质为白色固体,而铁粉是黑色的,因此保鲜剂一定不是铁粉;只可能是生石灰;
与水反应的化学方程式为:CaO+H2O=Ca(OH)2 ;
根据碳酸钙遇盐酸放出气体,滤渣的试管中加入足量的稀盐酸,白色固体消失,有气泡产生,因此样品中还一定含有的物质是碳酸钙(或CaCO3);
向盛有滤液即氢氧化钙溶液的试管中通入二氧化碳气体,变浑浊,不能确定的物质是氢氧化钙(或熟石灰或Ca(OH)2)
[拓展应用]
充气包装的保鲜,对所充气体的基本要求为:无毒、无味、无嗅,化学性质稳定,廉价易获得;可以填充到食品包装内的气体如:氮气、二氧化碳;
故答案为:(1)氢氧化钠和浓硫酸都具有很强的腐蚀性;
(2)③(或Fe或铁粉);①生石灰(或CaO或氧化钙);CaO+H2O=Ca(OH)2 ;碳酸钙(或CaCO3);
氢氧化钙(或熟石灰或Ca(OH)2);
[拓展应用]
不与食品发生化学反应(或化学性质稳定);氮气(或N2、二氧化碳或CO2).
点评:解答这类题目时,首先要弄清题意,看看究竟是探究谁的成分,是食品干燥剂的、保鲜剂的,还是真空包装的;然后再顺藤摸瓜,按照相应的常见成分对号入座,并结合它的相关性质和用途,细心地进行思考分析或者实验探究即可.

练习册系列答案
相关题目

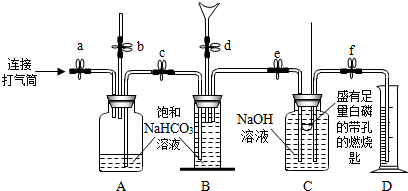
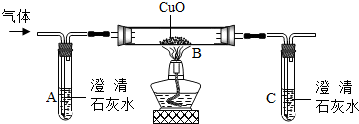 (2011?乐陵市二模)不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.
(2011?乐陵市二模)不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.