题目内容
【题目】将稀硫酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀硫酸的质量变化曲线如图所示: 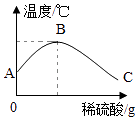
(1)写出该反应的化学方程式: .
(2)由图可知,稀硫酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”)反应.
(3)B点溶液中含有的溶质是 , C点的pH(填“>”“=”或“<”)7.
(4)生石灰溶于水也会放出热量,使生石灰溶于水放出热量的原因是(用化学方程式表示)
【答案】
(1)2NaOH+H2SO4=Na2SO4+2H2O
(2)放热
(3)硫酸钠;<
(4)CaO+H2O=Ca(OH)2
【解析】解:(1)氢氧化钠与硫酸反应生成硫酸钠和水;故填:2NaOH+H2SO4=Na2SO4+2H2O;(2)由图象可以看出,随着稀硫酸的加入,温度在逐渐的升高,说明稀硫酸与氢氧化钠溶液发生的反应是放热反应.故填:放热;(3)由图是可知,在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成硫酸钠和水,显中性;C点表示的溶液中硫酸已经过量,此时溶液的pH<7;故填:硫酸钠;<;(4)生石灰与水反应生成熟石灰,此过程会放出大量的热,故填:CaO+H2O=Ca(OH)2 .
【考点精析】解答此题的关键在于理解中和反应及其应用的相关知识,掌握中和反应:酸与碱作用生成盐和水的反应,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案【题目】在研究酸和碱的化学性质时,同学们想证明:稀H2SO4与NaOH溶液确实发生了反应.请你与他们一起完成实验方案设计、实施和评价.(注:硫酸钠溶液呈中性)
(1)向NaOH溶液中滴入2﹣3滴酚酞溶液,溶液由无色变为色. 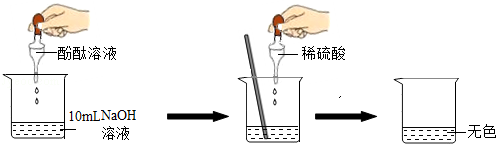
(2)根据上述实验中颜色变化,确定稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为 .
(3)因为溶液变成了无色,小林说“稀硫酸一定过量了”,小林这么说的理由是 .
(4)为确定小林的说法是否正确,同学们又设计了下列实验方案并进行实验:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀H2SO4过量 |
方案二 | 取样,滴入2﹣3滴紫色石蕊溶液 | 溶液变成红色 | 稀H2SO4过量 |
上述方案中,你认为正确的是(填“方案一”或“方案二”).
另外一个实验方案错误的原因(用化学方程式表示): .
请你再设计一种实验方案确定稀H2SO4过量,你选用(填药品).