题目内容
【题目】某同学要测定碳酸钙粉末与稀盐酸反应生成二氧化碳的质量,设计了两个实验方案。(假设二氧化碳全部从溶液中逸出)
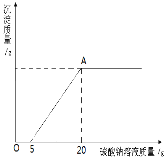
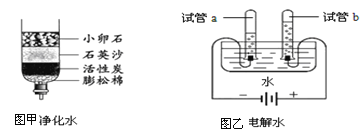
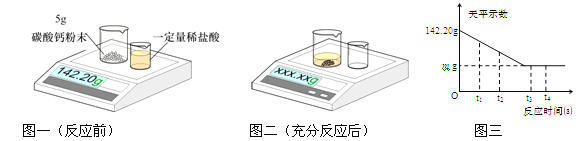
【方案一】如图一所示,将小烧杯中的稀盐酸倒入盛有5g碳酸钙粉末的大烧杯中,记录天平的示数直至充分反应(如图二)。天平示数与反应时间的关系如图三所示。
① 发生反应的化学方程式是 (12) 。
② 分析图三可知t3时反应已停止,理由是 (13)。
③ 天平示数m的范围是 (14) 。
【方案二】用下图装置实验也可知生成二氧化碳的质量(装置气密性良好)。下列分析错误的是 (15) 。
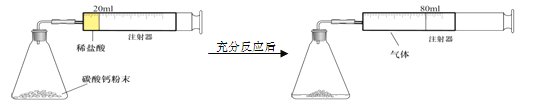
A、通过测定二氧化碳的体积计算二氧化碳的质量
B、注射器中收集到的气体是CO2
C、共生成了80 mL CO2
D、反应前后整个装置的质量不变
【答案】(12)CaCO3 + 2HCl → CaCl2 +H2O +CO2↑ (13)质量不再变小
(14)140.00 g<m<142.20g (15)BC
【解析】
试题分析:【方案一】① 发生反应的化学方程式是CaCO3 + 2HCl → CaCl2 +H2O +CO2↑;② 图三可知t3时反应已停止,理由是质量不再变小;③因为充分反应,碳酸钙可以反应完,反应完产生的气体的质量为:CaCO3 + 2HCl → CaCl2 +H2O +CO2↑
100 44
5g 2.2g
也可以有剩余,故 天平示数m的范围是140.00 g<m<142.20g【方案二】用下图装置实验也可知生成二氧化碳的质量(装置气密性良好)。分析错误的是B、注射器中收集到的气体是CO2是错误的叙述,因为先进入注射器得为装置内的空气;C、共生成了80 mL CO2是错误的叙述;因为开始有20ml的稀盐酸。

练习册系列答案
相关题目