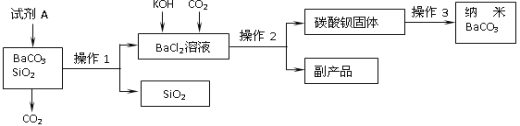
题目内容
【题目】(6分)【实验探究】
(1)请你依据下图设计一个酸和碱反应的探究实验:
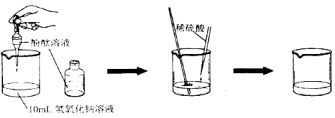
实验步骤 | 实验现象 | 结论 |
①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液 ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液。 | ①溶液颜色 ; ②不断搅拌溶液至溶液颜色变成 色。 | 酸和碱发生了中和反应 |
(2)为探究上述酸、碱反应后硫酸是否过量,甲、乙、丙三位同学设计了以下方案:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
甲同学的方案 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
乙同学的方案 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好完全反应 |
丙同学的方案 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
【实验评价】
①三个方案中只有 是正确的(填“甲”、“乙”、“丙”)。
②请分析另外两个同学方案错误的原因:
一个错误的原因是 ,
另一个错误的原因是 。
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂
【答案】【实验探究】(1)实验现象:① 变成红色 ② 无色。
(2)【实验评价】① 丙 ② 硫酸钠溶液也能与氯化钡反应生成白色沉淀 酚酞遇酸也不变色
【实验反思】 Zn
【解析】
试题分析:【实验探究】(1) ①无色酚酞遇碱溶液变红色,遇酸溶液不变色,所以向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液,溶液颜色变红,②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液,发现溶液变为无色,可得出结论:酸和碱发生了中和反应
(2)【实验评价】①三个方案中只有丙是正确的,另外两个同学方案错误的原因,甲同学错误的原因是:因为溶液中还有生成的硫酸钠,而硫酸钠溶液也能与氯化钡反应生成白色沉淀,所以无法确定是否含有硫酸,乙同学错误的原因:酚酞不仅在中性溶液中不变色,遇酸也不变色
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,实际就是抓住硫酸的化学性质,所以还可选择一种试剂活泼金属,如锌或碳酸盐

 习题精选系列答案
习题精选系列答案