题目内容
【题目】某同学为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如下图所示的装置(图中的铁架台已略去),实验步骤如下:①按图连接好装置;②称取氢氧化钠样品2克,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中过量,关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液220mL。请回答下列问题: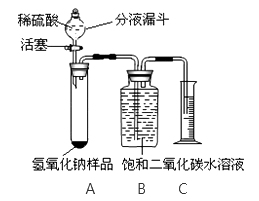
(1)判断氢氧化钠变质的实验现象是 , 氢氧化钠变质的原因是 , 因此,实验中氢氧化钠必须保存。
(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是 。
(3)B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是。
(4)判断步骤③中滴入的稀硫酸已过量的标志是。
(5)氢氧化钠样品中的碳酸钠的质量分数为。(CO2的密度约为2.0g /L,二氧化碳的体积等于排出的饱和二氧化碳水溶液的体积。)
(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是。
【答案】
(1)A中有气泡产生;空气中含有二氧化碳,能与它反应;密封
(2)检查装置的气密性
(3)二氧化碳能溶于水
(4)加入稀硫酸时没有气泡产生
(5)53%
(6)氢氧化钠具有潮解性,变质的固体中除碳酸钠外,还含有水
【解析】(1)判断氢氧化钠变质的实验现象是A中有气泡产生,氢氧化钠变质的原因是空气中含有二氧化碳,能与它反应。因此,实验中氢氧化钠必须密封保存。(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是检查装置的气密性。(3)B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是二氧化碳能溶于水。(4)判断步骤③中滴入的稀硫酸已过量的标志是加入稀硫酸时没有气泡产生。(5)氢氧化钠样品中的碳酸钠的质量分数为∶生成二氧化碳质量是0.220L×2.0g /L=0.44g.Na2CO3 →CO2 ,106→44, ![]() =
= ![]() ,x=1.06g,
,x=1.06g, ![]() ×100%=53%.(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是氢氧化钠具有潮解性,变质的固体中除碳酸钠外,还含有水。
×100%=53%.(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是氢氧化钠具有潮解性,变质的固体中除碳酸钠外,还含有水。
故答案为:(1)A中有气泡产生;空气中含有二氧化碳,能与它反应;密封(2)检查装置的气密性(3)二氧化碳能溶于水(4)加入稀硫酸时没有气泡产生(5)53%(6)氢氧化钠具有潮解性,变质的固体中除碳酸钠外,还含有水(1)根据氢氧化钠与二氧化碳会变质生成碳酸钠,滴入盐酸会有气泡产生分析
(2)在试验过程中有气体参与,必须保证装置的气密性
(3)二氧化碳易溶于水
(4)若氢氧化钠变质则会生成气体,不在产生气体说明反应完毕
(5)根据二氧化碳的质量可以求出碳酸钠的质量,进而求出质量分数
(6)根据氢氧化钠易吸水潮解分析解答

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案